题目内容
2. 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
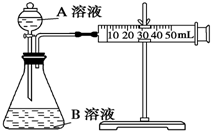
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.(1)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
| 序号 | A | B |
| 1 | 2ml0.1mol/LH2C2O4溶液 | 4ml0.01mol/LKMnO4溶液 |
| 2 | 2ml0.2mol/LH2C2O4溶液 | 4ml0.01mol/LKMnO4溶液 |
| 3 | 2ml0.2mol/LH2C2O4溶液 | 4ml0.01mol/LKMnO4溶液和少量MnSO4溶液 |
(2)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小.
取两支试管各加入2mL 0.1mol/L H2C2O4溶液,另取两支试管各加入4mL 0.1mol/L KMnO4溶液.将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对化学反应速率的影响,但该组同学始终没有看到溶液明显褪色,其原因是KMnO4溶液过量.
分析 (1)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大;对比②③实验可探究催化剂对化学反应速率的影响,③中使用了催化剂;反应速率快,相同时间内收集到的二氧化碳越多;
(2)其他条件相同,只是在不同温度下反应得出实验目的;草酸和高锰酸钾反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,分析数据可知高锰酸钾过量.
解答 解:(1)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大,
对比②③实验可探究催化剂对化学反应速率的影响,③中使用了催化剂,故相同时间内③的反应速率最快,实验中所得二氧化碳最多,
所以该实验目的为探究浓度和催化剂对反应速率的影响;在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序为:③>②>①,
故答案为:浓度和催化剂; ③>②>①;
(2)从题中可知其他条件相同,只是在不同温度下反应,所以该实验探究的是温度对反应速率的影响;
草酸和高锰酸钾反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
草酸的物质的量为:0.002L×0.1mol•L-1=2×10-4mol,
高锰酸钾的物质的量为:0.004L×0.1mol•L-1=4×10-4mol,
由方程式可知,高锰酸钾过量,故没看到溶液完全褪色,
故答案为:温度;KMnO4溶液过量.
点评 本题考查了探究影响化学反应速率的因素方法,注意掌握浓度、温度、催化剂对化学反应速率的影响,试题侧重考查学生的分析、理解能力及化学实验能力,题目难度中等.

练习册系列答案
相关题目
2.下列对分子性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 由于乳酸( )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体 | |
| C. | HF的稳定性很强,是因为其分子间能形成氢键 | |
| D. | 由右图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子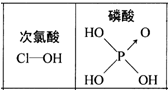 |
3.下列叙述错误的是( )
| A. | 用AgNO3溶液可以鉴别KCl和KI | |
| B. | SO2使溴水褪色与乙烯使KMnO4溶液褪色原理相同 | |
| C. | 可根据硫酸密度的大小判断铅蓄电池是否需要充电 | |
| D. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
10.下列有关中和滴定的操作:①用标准液润洗滴定管;②往滴定管内注入标准溶液,排气泡并调零;③检查滴定管是否漏水;④滴定;⑤滴加2-3滴指示剂于锥形瓶的待测液中;⑥用水洗涤.正确的操作顺序是( )
| A. | ③⑥①②⑤④ | B. | ⑤①②⑥④③ | C. | ⑤④③②①⑥ | D. | ③①②④⑤⑥ |
17. 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
(1)向锥形瓶中移取一定体积的白醋所用的仪器是酸式滴定管,该实验应选用酚酞作指示剂,达到滴定终点的实验现象是:锥形瓶由无色变为浅红色且半分钟内不复原.
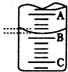
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为25.40mL.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是CD
A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式:C=$\frac{c×(25.35+25.30)}{2V}$.
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为25.40mL.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式:C=$\frac{c×(25.35+25.30)}{2V}$.
7.下列括号内有关物质的描述及用途错误的是( )
| A. | 硅(半导体材料) | B. | 二氧化硅(制光导纤维) | ||
| C. | Na2Si03 (用作粘合剂,俗称水玻璃) | D. | Al(OH)3(用作胃药,俗称人造刚玉) |
11.下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是( )
| A. | 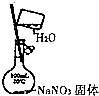 配置一定物质的量 浓度的NaNO3溶液 | |
| B. | 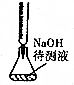 中和滴定 | |
| C. | 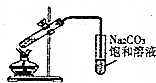 制备乙酸乙酯 | |
| D. | 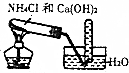 实验室制取氨 |
12.某固体化合物A不导电,但熔化或溶于水都能完全电离.下列关于物质A的说法中,正确的是( )
| A. | A是非电解质 | B. | A是强电解质 | C. | A是共价化合物 | D. | A是弱电解质 |
