题目内容
下列事实、离子方程式及其对应关系均正确的是( )
| A、铁溶于稀硝酸溶液变为浅绿色:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| B、向K2Cr2O7溶液中滴加少量浓H2SO4,溶液变为黄色:Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+ |
| C、向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2═2I2+2H2O |
| D、向水杨酸 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.浅绿色为二价铁离子;
B.加入浓硫酸氢离子浓度增大;
C.发生氧化还原反应生成碘和水;
D.只有-COOH能与碳酸氢钠反应.
B.加入浓硫酸氢离子浓度增大;
C.发生氧化还原反应生成碘和水;
D.只有-COOH能与碳酸氢钠反应.
解答:
解:A.铁溶于稀硝酸溶液变为浅绿色:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,故A错误;
B.加入浓硫酸氢离子浓度增大,平衡左移,变为橙色,故B错误;
C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后变蓝的离子反应为4H++4I-+O2═2I2+2H2O,故C正确;
D.服用阿司匹林过量出现水杨酸(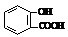 )反应,可静脉注滴NaHCO3溶液的离子反应为
)反应,可静脉注滴NaHCO3溶液的离子反应为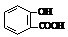 +HCO3-→
+HCO3-→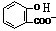 +CO2↑+H2O,故D错误.
+CO2↑+H2O,故D错误.
故选C.
B.加入浓硫酸氢离子浓度增大,平衡左移,变为橙色,故B错误;
C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后变蓝的离子反应为4H++4I-+O2═2I2+2H2O,故C正确;
D.服用阿司匹林过量出现水杨酸(
 )反应,可静脉注滴NaHCO3溶液的离子反应为
)反应,可静脉注滴NaHCO3溶液的离子反应为 +HCO3-→
+HCO3-→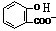 +CO2↑+H2O,故D错误.
+CO2↑+H2O,故D错误.故选C.
点评:本题考查离子反应方程式书写的正误判断,明确发生的化学反应是解答的关键,注意与量有关的离子反应为解答的难点,题目难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Cl2与足量Fe反应转移电子数为3NA |
| B、在1L 1mol?L-1的AlCl3溶液中,Cl-离子的数目小于3NA |
| C、1mol Na2O和Na2O2的混合晶体中含有的阴、阳离子总数是3NA |
| D、在某密闭容器中盛有0.1mol N2和0.3mol H2,在一定条件下充分反应后,可得0.2NA个NH3分子 |
下列有关实验装置进行的相应实验,不能达到实验目的是( )


| A、用图1所示装置除去Cl2中含有的少量HCl |
| B、用图2所示装置蒸发KCl溶液制备无水KCl |
| C、用图3所示装置可以完成“喷泉”实验 |
| D、用图4所示装置制取、收集干燥纯净的NH3 |
下列名称或化学式一定表示纯净物的是( )
| A、氯乙烯 |
| B、聚乙烯 |
| C、C3H7Cl |
| D、(C6H10O5)n |
将2mol H2和1mol CO2充入体积为10L的恒容密闭容器中,在一定条件下发生反应:
①CO2(g)+H2(g)?CO(g)+H2O(g)△H1=+41.2kJ?moL-1;
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-49kJ?moL-1.
反应100min后达到平衡,测得下表数据:
下列说法正确的是( )
①CO2(g)+H2(g)?CO(g)+H2O(g)△H1=+41.2kJ?moL-1;
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-49kJ?moL-1.
反应100min后达到平衡,测得下表数据:
| 温度 | 转化率(%) | 物质的量(mol) | ||
| H2 | CO2 | CH3OH | CO | |
| 240℃ | 10 | 0.05 | 0.05 | |
| A、升高温度,反应①的平衡常数减小 |
| B、升高温度,CH3OH的含量提高 |
| C、H2转化率为10% |
| D、100min内,反应②的速率为v(CO2)=0.0001mol?L-1?min-1 |
用Zn片、Cu片和稀硫酸组成的电池装置.下列有关该装置的说法不正确的是( )
| A、该装置将化学能转变为电能 |
| B、溶液中的阳离子向锌电极移动 |
| C、Cu极上有气泡产生,发生还原反应 |
| D、电流方向是从铜片流向锌片 |
 在不同温度下,反应CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数K如下表:
在不同温度下,反应CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数K如下表: (1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
(1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示: