题目内容
4.一定条件下,可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.12mol/L,则下列判断不正确的是( )| A. | 无法确定c1:c2的值 | B. | 平衡时,Y和Z的生成速率之比为3:2 | ||
| C. | 0.28mol/L<c1+c2+c3<0.56mol/L | D. | c1的取值范围为0<c1<0.14mol/L |
分析 X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol•L-1、0.3mol•L-1、0.08mol•L-1,利用极值转化;
A.可根据反应转化关系和平衡浓度计算初始浓度关系;
B.达到平衡状态时,正逆反应速率相等;
C.根据c1:c2的值结合各自的数值范围来计算判断;
D.根据可逆反应是不能完全转化的来分析.
解答 解:A.设X转化的浓度为x,
X(g)+3Y(g)?2Z(g)
初始浓度:c1 c2 c3
转化浓度:x 3x 2x
平衡浓度:0.1moL/L 0.3mol/L 0.12mol/L
则:c1:c2=(x+0.1moL/L):(3x+0.3mol/L)=1:3,故A错误;
B.平衡时,正逆反应速率相等,则Y和Z的生成速率之比为3:2,即2VY(正)=3VZ(逆)故B正确;
C.反应为可逆反应,物质不可能完全转化,如反应向正反应方向进行,则0<c1,如反应向逆反应方向进行,则c1<0.16mol•L-1,故有0<c1<0.16mol•L-1,c1:c2=1:3,故有0<c2<0.48mol•L-1,0<c1+c2<0.64mol/L,故C错误;
D.反应为可逆反应,物质不可能完全转化,如反应向正反应方向进行,则0<c1,如反应向逆反应方向进行,则c1<0.16mol•L-1,故有0<c1<0.16mol•L-1,故D错误.
故选B.
点评 本题考查学生可逆反应化学平衡的建立,可以正向进行建立,还可以逆向进行来建立,注意知识的整理和归纳是关键,难度不大.

练习册系列答案
相关题目
15.下列物质中只含有氯分子的是( )
| A. | 液氯 | B. | 氯水 | C. | 盐酸 | D. | 氯化铁 |
12.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.2 mol•L-1 FeCl3溶液中含有Cl-总数为0.6NA | |
| B. | 常温常压下,a mo1 O2与2a mo1 NO混合,降温得到混合气体中氧原子数小于4a NA | |
| C. | 2 mol NaHSO4晶体中含有阳离子的数目为4NA | |
| D. | 3g金刚石和4g石墨中的碳碳单键数目均为0.5NA |
19.将7g某铜、银合金与足量的a mol/L HNO3充分反应,完全溶解后放出的气体与标准状况下的氧气0.56L混合,通入水中恰好完全吸收,则此合金中铜的质量是( )
| A. | 1.6 g | B. | 2.4 g | C. | 3.2 g | D. | 4.8 g |
9.下列各组中的反应,属于同一反应类型的是( )
| A. | 由甲烷制一氯甲烷;由乙烯与氯化氢反应制一氯乙烷 | |
| B. | 由苯与浓硝酸和浓硫酸的混酸反应制硝基苯;由苯与液溴反应制溴苯 | |
| C. | 由乙醇制乙醛;由乙醇和乙酸反应制乙酸乙酯 | |
| D. | 由苯与氢气反应制环己烷;由淀粉水解制葡萄糖 |
13.化学与生产、生活密切相关.下列叙述不正确的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 葡萄糖注射液不能产生丁达尔效应,不属于胶体 | |
| C. | 蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生无关 |
14.有机物X的分子式为C7H14O2.其水解可得到CH3OH,则X的结构有(不考虑立体异构)( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
 利用Cu+2FeCl3=CuCl2+2FeCl2反应,设计一个原电池.
利用Cu+2FeCl3=CuCl2+2FeCl2反应,设计一个原电池.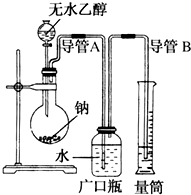 为了确定乙醇分子的结构简式是CH3-O-CH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子数目.试回答下列问题:
为了确定乙醇分子的结构简式是CH3-O-CH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子数目.试回答下列问题: