��Ŀ����
1�������Ͳ�������Fe������ͨ�Ļ�ԭ���������кܴ�IJ��죬����Fe�۱�������г�ǿ�Ĵ��ԣ����������ܶȴż�¼�Ľ����Լ���Ч�����ȣ�ʵ���Ҳ������ԭ���Ʊ�����Fe����������ͼ1��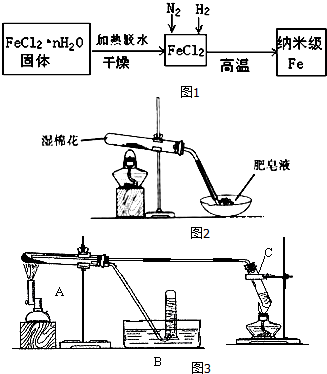
��1����������Fe�Ļ�ѧ����ʽΪFeCl2+H2$\frac{\underline{\;����\;}}{\;}$Fe+2HCl��
��2������Fe���ڿ���������ȼ�ɺ�ɫ���壬���������е���˿�������ڿ����м���Ҳ����ȼ�գ���ԭ��������Fe��������Ӵ����Ӧ���ʿ죮
��3��FeCl2•nH2O���������ˮͨ��Ҫͨ������HCl������������HCl����FeCl2ˮ�⣬��ͨ���HCl����ɴ���ˮ������
�������ϣ��ڲ�ͬ�¶��£�����Fe����ˮ������Ӧ�Ĺ�����ﲻͬ���¶ȵ���570��ʱ����FeO������570��ʱ����Fe3O4��
��ͬѧ����ͼ2��ʾװ�ý�������Fe����ˮ������ʵ�飺
��4����װ��������Fe����ˮ������Ӧ�Ļ�ѧ����ʽ��Fe+H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$FeO+H2��
��ͬѧ����ͼ3��ʾװ�ý�������Fe����ˮ�����ķ�Ӧ����֤���
��5��װ��C����������ȡˮ������
��6����ͬѧΪ̽��ʵ��������Թ��ڵĹ������ʳɷ֣����������ʵ�飺
| ʵ�鲽�� | ʵ����� | ʵ������ |
| �� | ����Ӧ��õ���ɫ��ĩX���ٶ�Ϊ���ȵģ���ȡ������������һ�Թ��У������������ᣬ�� | ��ɫ��ĩ���ܽ⣬��Һ��dz��ɫ�����������ݲ��� |
| �� | ��ʵ��I�еõ�����Һ�μӼ���KSCN��Һ���� | ��Һû�г���Ѫ��ɫ |
��7����ͬѧ��ȡ5.60gFe�ۣ����ҵ�װ�÷�Ӧһ��ʱ���ֹͣ���ȣ����Թ��ڵĹ��������ڸ���
������ȴ�Ƶ�����Ϊ6.88g��Ȼ����ȴ��Ĺ�������������FeCl3��Һ��ַ�Ӧ������FeCl3
��0.08mol����ͬѧʵ��Ĺ������ΪFe3O4��
���� I�����ᾧˮ���Ȼ�����������ˮ�õ�FeCl2��N2��H2��FeCl2�ڸ��������µõ�����Fe�������Ļ�ѧ��ӦΪFeCl2+H2$\frac{\underline{\;����\;}}{\;}$Fe+2HCl��
��1����������ͼ��֪���ڸ�����������������ԭ�Ȼ������ɵ�����Fe��
��2����Ӧ���ʱ����Խ��Ӧ����Խ�죻
��3��FeCl2•nH2O���������ˮʱ������������ˮ�������������������Ȼ��⣬Ϊ��ֹˮ����Խ�����HCl��Χ�м��ȣ�
II����4��Fe����ˮ�����ڼ��������·�Ӧ����FeO��������
��5��װ��C�����Ʊ�ˮ������
��6�������۹�������������Fe3+��
��7������ˮ������Ӧ������������������������Ϲ������������ж�������ɷ֣�
��� �⣺I�����ᾧˮ���Ȼ�����������ˮ�õ�FeCl2��N2��H2��FeCl2�ڸ��������µõ�����Fe�������Ļ�ѧ��ӦΪFeCl2+H2$\frac{\underline{\;����\;}}{\;}$Fe+2HCl��
��1����������ͼ��֪���ڸ�����������������ԭ�Ȼ������ɵ�����F����Ӧ����ʽΪFeCl2+H2$\frac{\underline{\;����\;}}{\;}$Fe+2HCl���ʴ�Ϊ��FeCl2+H2$\frac{\underline{\;����\;}}{\;}$Fe+2HCl��
��2������Fe��������Ӵ������Ӧ���ʿ죬��������Fe���ڿ���������ȼ�ɺ�ɫ���壬�����е���˿�����۱������С�����Ժ��ѷ�Ӧ��
�ʴ�Ϊ������Fe��������Ӵ������Ӧ���ʿ죻
��3��FeCl2•nH2O���������ˮͨʱ������������ˮ�������������������Ȼ��⣬Ϊ��ֹFeCl2ˮ�⣬FeCl2•nH2O���������ˮͨ��Ҫͨ������HCl���壬HCl������FeCl2ˮ�⣬��ͨ���HCl����ɴ���ˮ����������FeCl2•nH2O������ˮ��
�ʴ�Ϊ�������HCl���壻 HCl������FeCl2ˮ�⣬��ͨ���HCl����ɴ���ˮ������
��4��Fe����ˮ�����ڼ��������·�Ӧ����FeO������������ʽΪFe+H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$FeO+H2��
�ʴ�Ϊ��Fe+H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$FeO+H2��
��5����Ӧ��Ϊ����ˮ��������װ��C�����Ʊ�ˮ�������ʴ�Ϊ����ȡˮ������
��6�������۹�������������������Ӧ�����������ӣ���Ӧ����ʽΪ��2Fe3++Fe=3Fe2+������ȷ���Ƿ�ΪFeO���ʴ�Ϊ��2Fe3++Fe=3 Fe2+��
��7��3Fe+4H2O�TFe3O4 +4H2 Fe������Ϊ5.6g����n��Fe��=0.1mol�������ЩFe��ȫ��ˮ������Ӧ����ôӦ������$\frac{0.1}{3}$mol ��Fe3O4��m��Fe3O4��=$\frac{0.1}{3}$��M��Fe3O4��=7.73g����������ֻ������ 6.88g �� ���壬�ͱ��� Fe û����ȫ��Ӧ������ʣ�࣬��������ΪFe3O4��
�ʴ�Ϊ��Fe3O4��
���� ���⿼�������Ʊ���Ϊ��Ƶ���㣬�漰����ʽ�ļ��㡢������ԭ��Ӧ�����ӷ�Ӧ����Ӧ����Ӱ�죬������ѧ���ķ���������ʵ�������ͼ��������Ŀ��飬���ո���������ˮ��Ӧ��ʵ����װ�õ�����Ϊ���Ĺؼ�����Ŀ�Ѷ��еȣ�

| A�� | NaOH��Һ | B�� | AgNO3��Һ | C�� | Ba��OH��2��Һ | D�� | BaCl2��Һ |
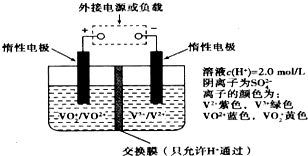 ����Դ�ͻ�����ѹ���£�����Դ�綯�������ɽ���Ϊδ�������ķ�չ��������綯������ʹ�����ͷ���أ�һ���Գ��3-5���Ӻ����������ɴ�1000������ɱ����ֻ��Ŀǰ﮵�ص�40%������������ֱ���﮵�ص�$\frac{1}{25}$��$\frac{1}{10}$��ȫ��Һ�����ܵ�������ò�ͬ��̬���ӶԵ�������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת����װ�ã���ԭ����ͼ��ʾ�������йظ÷���ص�˵������ȷ���ǣ�������
����Դ�ͻ�����ѹ���£�����Դ�綯�������ɽ���Ϊδ�������ķ�չ��������綯������ʹ�����ͷ���أ�һ���Գ��3-5���Ӻ����������ɴ�1000������ɱ����ֻ��Ŀǰ﮵�ص�40%������������ֱ���﮵�ص�$\frac{1}{25}$��$\frac{1}{10}$��ȫ��Һ�����ܵ�������ò�ͬ��̬���ӶԵ�������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת����װ�ã���ԭ����ͼ��ʾ�������йظ÷���ص�˵������ȷ���ǣ�������| A�� | �������У�H+����ͨ�����ӽ���Ĥ�����ƶ����γɵ���ͨ·�����Ҳ���缫��Ӧ | |
| B�� | �ŵ�����У��Ҳ���Һ����Һ��ɫ����ɫ��Ϊ��ɫ | |
| C�� | �õ��Ϊ�����أ��������Һ���ɻƱ���ʱ��Ϊ�����̣���ʱ�����ҺpHֵ���� | |
| D�� | ���ʱ��ת�Ƶĵ�����Ϊ3.01��1023���������Һ��n��H+��������0.5mol |
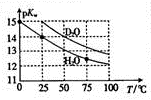 Hz0��D20��pKw ��pKw=-lgKw�����¶ȵĹ�ϵ��ͼ��ʾ�������й�˵����ȷ���ǣ�������
Hz0��D20��pKw ��pKw=-lgKw�����¶ȵĹ�ϵ��ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | D20�ĵ������Ϊ���ȹ��� | B�� | 25��ʱ����D20��pH����7 | ||
| C�� | 25��ʱ��pH=7��Һ��һ���Ǵ�H20 | D�� | �����£���Dz0�м���DCI��pKw��� |
 �����������ʵ���Ҫ���������ʽṹ����ش��������⣮
�����������ʵ���Ҫ���������ʽṹ����ش��������⣮��1����֪A��BΪ��������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ����������ʾ��
| ������/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
��2��ʵ��֤����KCl��MgO��CaO��TiN��4�־���Ľṹ��NaCl����ṹ���ƣ���ͼ1��ʾ������֪3�����Ӿ���ľ��������������
| ���Ӿ��� | NaCl | KCl | CaO |
| ������/kJ•mol-1 | 786 | 715 | 3401 |
��3�����������Ӻ�δ�ɶԵ���Խ�࣬�����Խ�ż�¼����Խ�ã�������������V2O5��CrO2�У��ʺ���¼�����ŷ�ԭ�ϵ���CrO2��
��4��ij�����ķ��ӽṹ��ͼ2��ʾ��������ڲ�����AC������ţ���
A�����Ӽ� B�����Լ� C��������
D����λ�� E����� F���Ǽ��Լ���
��1��Aװ��Ϊ���ȷֽ�����װ�ã���װ�ô������Թܿ�Ӧ������б��Cװ����ʢ�ŵ��Լ���Ũ���� ���ѧʽ����Eװ�õ������ǰ�ȫƿ�������������
��2��ʵ��������漰�����²������ٵ�ȼA���ľƾ��� ��Ϩ��A���ľƾ��� �۵�ȼD���ľƾ��� ��Ϩ��D���ľƾ��ƣ���4���������ȵ����˳��Ϊ�٢ۢܢڣ�����ţ�����ȼD���ƾ���ǰ����Ҫ���еIJ����������鴿��
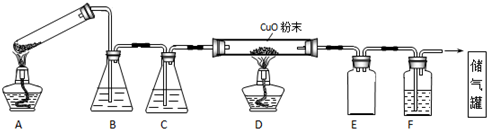
��3�������Ը��������Һ�ζ����ᾧ�壬��x��ֵ��
ʵ�鲽�裺ȷ��ȡ1.17g ���ᾧ�壬���100mL��Һ��ȡ��20.00mL����ƿ�У�����ƿ�м�������ϡH2SO4����0.0500mol/L���Ը��������Һ�ζ����ζ����յ�ʱ���ĸ��������Һ16.00mL���ζ�ʱ���������ķ�ӦΪ��2MnO4-+5H2C2O4+6H+�T10CO2+2Mn2++8H2O��
�����Ʋ�����Һ����Ҫ���������ձ�����һ����Ҫ�IJ���������100mL����ƿ����ͷ�ιܣ�
��x=1.5��
��4��Ϊ̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죬�ڼ����Թ��зֱ������������
| �Թ� | 0.01mol/L KMnO4 | 0.1mol/L H2C2O4 | 0.1mol/L H2SO4 | MnSO4���� |
| �� | 4mL | x mL | 1mL | �� |
| �� | y mL | 2mL | 1mL | �� |
��1����FeBr2��Һ�еμ�������ˮ����Һ��ƣ�����Ϊʹ��Һ��Ƶ����������Fe3+����ʵ��֤����Ĺ۵㣬����ʵ�����������ȡ������Ӧ�����Һ�μ�KSCN��Һ��죮
��2����֪������һЩ����ʵ�������ݼ��±���
| H2CO3 | K${\;}_{{a}_{1}}$=4.3��10-7 | HClO | Ka=2.95��10-8 |
| K${\;}_{{a}_{2}}$=5.61��10-11 | AgCl | Ksp=1.77��10-10 | |
| CH3COOH | Ka=1.76��10-5 | Ag2CrO4 | Ksp=1.12��10-12 |
����Ũ�Ⱦ�Ϊ0.010mol/L��NaCl��Na2Cr04��ɵĻ����Һ����μ���Ũ��Ϊ0.010mol•L-1AgN03��Һ���������ɵij����仯ѧʽΪAgCl��
��3���ֱ����ķݸ�100mL��Ũ�Ⱦ�Ϊ2mo1L-1��FeC13��Һ�У���������ͭ��ɵľ��ȷ�ĩ״�����õ��������ݣ�
| I | �� | �� | �� | |
| FeCl3��Һ���/mL | 100 | 100 | 100 | 100 |
| �����ĩ����/g | 3 | 6.6 | 9 | 12 |
| ʣ���ĩ����/g | 0 | 0.64 | 3.2 | 6.4 |
�ڸ��ݱ��е����ݷ���I��Ӧ�����Һ�д��ڵĽ����������С������ӷ��ű�ʾ��Fe3+��Fe2+��Cu2+��
 ��ͼ��ʾA--E �������ʵ��ת����ϵ������AΪ����ɫ��ĩ��CΪ���ʣ�DΪ���ӻ����
��ͼ��ʾA--E �������ʵ��ת����ϵ������AΪ����ɫ��ĩ��CΪ���ʣ�DΪ���ӻ����