题目内容
18.在一定的温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原来的温度,下列说法正确的是( )| A. | 溶液中Na+浓度增大,有O2放出 | B. | 溶液中OH-总数不变,有O2放出 | ||
| C. | 溶液的pH增大,有O2放出 | D. | 溶液中Na+总数减少,有O2放出 |
分析 过氧化钠能与水反应,则饱和的烧碱溶液中的溶剂减少,原饱和溶液有晶体析出,剩余溶液还是饱和溶液,温度不变时,溶液中离子的浓度不变,但数目减少.
解答 解:因过氧化钠与水反应生成氢氧化钠和氧气,因为已经饱和,所以不会再溶解,浓度不变,但由于水的减少,水中Na+、OH-的数目减少.
A、原饱和溶液有晶体析出,剩余溶液还是饱和溶液,温度不变时,溶液中离子的浓度不变,即溶液中钠离子浓度不变,有O2放出,故A错误;
B、溶液中OH-的数目减少,有O2放出,故B错误;
C、原饱和溶液有晶体析出,剩余溶液还是饱和溶液,温度不变时,溶液中离子的浓度不变,即溶液中OH-浓度不变,溶液的pH不变,有O2放出,故C错误;
D、溶液中Na+总数减少,有O2放出,故D正确.
故选D.
点评 本题考查过氧化钠与水的反应及饱和溶液的变化,明确饱和溶液中溶剂减少对溶液的影响是解答本题的关键,应抓住温度不变,饱和溶液析出晶体后剩余溶液仍然为饱和溶液来解答.

练习册系列答案
相关题目
8.下列反应的生成物为纯净物的是( )
| A. | 甲烷和氯气光照 | B. | 氯乙烯的加聚 | ||
| C. | 丙烯和氯化氢加成 | D. | 乙烯和水加成 |
9.下列装置或操作不能达到实验目的是( )
| A. |  比较 Cl2、Fe3+、I2的氧化性 | B. |  制取 Fe(OH)2 制取 Fe(OH)2 | ||
| C. | 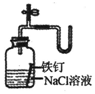 证明铁生锈时空气参加反应 | D. | 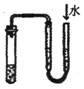 检查装置气密性 |
6.室温下某溶液中由水电离出的H+浓度为1.0×10-13mol•L-1,则在此溶液中一定不可能大量存在的离子组是( )
| A. | Al3+、K+、NO3-、Cl- | B. | K+、Na+、HCO3-、Cl- | ||
| C. | Na+、CO32-、SO42-、NO3- | D. | Ba2+、Na+、Cl-、NO3- |
3.有机物R的分子式为C5H12O,能与乙酸发生酯化反应,则R的结构有( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
7. 通过膜电池可除去废水中的乙酸钠和对氯笨酚(
通过膜电池可除去废水中的乙酸钠和对氯笨酚( ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )
 通过膜电池可除去废水中的乙酸钠和对氯笨酚(
通过膜电池可除去废水中的乙酸钠和对氯笨酚( ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )| A. | B为电池的正极,发生还原反应 | |
| B. | 电流方向从B极沿导线经小灯泡流向A极 | |
| C. | A极的电极反应式为 +e-═Cl-+ +e-═Cl-+ | |
| D. | 当外电路中有0.2mole-转移时,A极区增加的H+的数目为0.1NA |
1.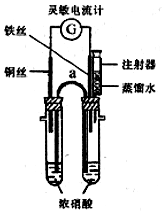 某化学课外活动小组的同学利用原电池原理探究一定温度下(实验时实际的环境温度)使铁钝化的硝酸的最低浓度.
某化学课外活动小组的同学利用原电池原理探究一定温度下(实验时实际的环境温度)使铁钝化的硝酸的最低浓度.
实验步骤如下:
①向两支具支试管中分别加入浓硝酸5.0mL(质量分数为65%,密度为1.4g/mL).按图组装好实验装置.
②将铜丝和铁丝同时插入浓硝酸中,观察到灵敏电流计指针先指向铜丝,但又迅速反转(只需1-2s)指向铁丝一端.
③用盛有5.0mL蒸馏水的注射器向具支试管内加水,并注视电流计的指针偏转方向.在指针恰好发生反转又指向铜丝时停止实验,记录此时已注入的水的体积.
重复三次实验获得的数据如下:
请回答下列问题:
(1)在该装置中仪器a因其作用而称为盐桥;指针指向铁丝时,铁丝为正极(填“正”或“负”)
(2)65%的硝酸的物质的量浓度是14.4mol/L;在未注水前正极的电极反应式为NO3-+e-+2H+=NO2↑+H2O.
(3)T1=T2(填“>”、“<”或“=”)
(4)在本实验温度下,使铁钝化的硝酸最低浓度为48%;利用本实验数据判断,若以45%的硝酸进行实验(不再注水),则电流表的指针应指向电极(填“铁”或“铜”)
(5)该实验装置上的不足是缺少尾气处理装置,改进方法是应在两侧支管口处均连接导管,将产生的气体导入盛有氢氧化钠溶液的烧杯中.
 某化学课外活动小组的同学利用原电池原理探究一定温度下(实验时实际的环境温度)使铁钝化的硝酸的最低浓度.
某化学课外活动小组的同学利用原电池原理探究一定温度下(实验时实际的环境温度)使铁钝化的硝酸的最低浓度.实验步骤如下:
①向两支具支试管中分别加入浓硝酸5.0mL(质量分数为65%,密度为1.4g/mL).按图组装好实验装置.
②将铜丝和铁丝同时插入浓硝酸中,观察到灵敏电流计指针先指向铜丝,但又迅速反转(只需1-2s)指向铁丝一端.
③用盛有5.0mL蒸馏水的注射器向具支试管内加水,并注视电流计的指针偏转方向.在指针恰好发生反转又指向铜丝时停止实验,记录此时已注入的水的体积.
重复三次实验获得的数据如下:
| 实验次数 | 实验温度(℃) | 注入水的体积(mL) |
| 1 | 17.2 | 2.4 |
| 2 | T1 | 2.5 |
| 3 | T2 | 2.3 |
(1)在该装置中仪器a因其作用而称为盐桥;指针指向铁丝时,铁丝为正极(填“正”或“负”)
(2)65%的硝酸的物质的量浓度是14.4mol/L;在未注水前正极的电极反应式为NO3-+e-+2H+=NO2↑+H2O.
(3)T1=T2(填“>”、“<”或“=”)
(4)在本实验温度下,使铁钝化的硝酸最低浓度为48%;利用本实验数据判断,若以45%的硝酸进行实验(不再注水),则电流表的指针应指向电极(填“铁”或“铜”)
(5)该实验装置上的不足是缺少尾气处理装置,改进方法是应在两侧支管口处均连接导管,将产生的气体导入盛有氢氧化钠溶液的烧杯中.
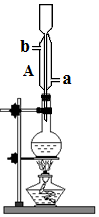 将无水乙醇、冰醋酸、浓硫酸放入烧瓶中,并加入沸石,加热一段时后,再更换装置可蒸馏出乙酸乙酯.
将无水乙醇、冰醋酸、浓硫酸放入烧瓶中,并加入沸石,加热一段时后,再更换装置可蒸馏出乙酸乙酯.
 .
.