题目内容
下列反应处于平衡状态,2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,以下措施使平衡向右移动的是:①降低温度; ②增大压力; ③加入氧气; ④去掉部分三氧化硫;⑤恒压时通入少量N2( )
| A、①②③④ | B、②③④⑤ |
| C、②④⑤ | D、全部 |
考点:化学平衡的影响因素
专题:
分析:正反应为气体体积减小的放热反应,若使反应正向移动,除增大反应物浓度和减小生成物浓度外还可以加压和降温,据此分析.
解答:
解:正反应为气体体积减小的放热反应,若使反应正向移动,除增大反应物浓度和减小生成物浓度外还可以加压和降温,
①降温,平衡正向移动,故正确;
②加压平衡正向移动,故正确;
③加入反应物氧气,平衡正向移动,故正确;
④去掉部分生成物,平衡正向移动,故正确;
⑤恒压通入氮气,平衡向气体体积增大的逆向移动,故错误;
故选A.
①降温,平衡正向移动,故正确;
②加压平衡正向移动,故正确;
③加入反应物氧气,平衡正向移动,故正确;
④去掉部分生成物,平衡正向移动,故正确;
⑤恒压通入氮气,平衡向气体体积增大的逆向移动,故错误;
故选A.
点评:本题考查了影响平衡移动的因素,题目难度不大.

练习册系列答案
相关题目
利用下列实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤作用的活性物质.下列说法错误的是( )
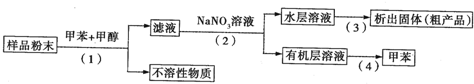

| A、步骤(1)需要过滤装置 |
| B、活性物质易溶于有机溶剂,难溶于水 |
| C、步骤(3)需要用到蒸发皿 |
| D、步骤(4)是利用物质的沸点差异进行分离的 |
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法.流程如下下列有关说法正确的是( )
CrOH42-
Cr2O72-→
Cr3+
Cr(OH)3↓
其中第①步中存在平衡:2CrO42-(黄色)+2H+???Cr2O72-(橙色)+H2O.
CrOH42-
| H+ |
| ①转化 |
| Fe2+ |
| ②还原 |
| 沉淀剂 |
| ③沉淀 |
其中第①步中存在平衡:2CrO42-(黄色)+2H+???Cr2O72-(橙色)+H2O.
| A、第①步当2v(Cr2O72-)=v(CrO42-)时,达到了平衡状态 |
| B、对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C、常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至9 |
| D、第②步中,还原0.1 mol Cr2O72-需要91.2 g FeSO4 |
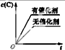
如图是某温度时N2与H2反应过程中的能量变化曲线图,下列叙述中不正确的是( )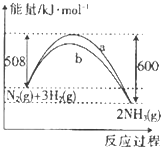

| A、该反应的热化学方程式为N2(g)+3H2(g)?2NH2(g)△H=-92KJ/mol |
| B、b曲线是加入催化剂时的能量变化曲线 |
| C、只加入催化剂不改变化学反应的反应热 |
| D、在一定条件下,2molN2(g)和6molH2(g)通入某密闭容器中,反应后放出的热量为184KJ |
以下现象中,不属于蛋白质变性的是( )
| A、用波尔多液杀菌 |
| B、用福尔马林对种子消毒 |
| C、鸡蛋白溶液中加入食盐变浑浊 |
| D、用酒精消毒医疗器械 |
下列所得溶液的物质的量浓度等于0.1mol?L-1的是( )
| A、将0.1 mol氨充分溶解在1 L水中 |
| B、将10 g质量分数为98%的硫酸与990 g水混合 |
| C、将8 g三氧化硫溶于水并配成1 L溶液 |
| D、将0.1 mol氧化钠溶于水并配成1 L溶液 |