题目内容
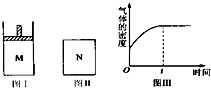 在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ)中,分别加入a mol A和a mol B,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?xC(g)△H<0,平衡时M中A、B、C的物质的量之比为1:3:4,下列判断不正确的是( )
在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ)中,分别加入a mol A和a mol B,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?xC(g)△H<0,平衡时M中A、B、C的物质的量之比为1:3:4,下列判断不正确的是( )| A、x=4 |
| B、若N中气体的密度如图Ⅲ所示,则A、B只有一种是气态 |
| C、若A为气体,B为非气体,则平衡时M、N中C的物质的量相等 |
| D、若A、B均为气体,平衡时M中A的转化率大于N中A的转化率 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、利用三段式,根据化学方程式计算出X的值;
B、恒容条件下,根据密度可判断出反应前后气体的质量的变化,进而确定物质的状态;
C、根据等效平衡的特征判断;
D、根据压强对平衡的影响判断.
B、恒容条件下,根据密度可判断出反应前后气体的质量的变化,进而确定物质的状态;
C、根据等效平衡的特征判断;
D、根据压强对平衡的影响判断.
解答:
解:A、利用三段式,设转化了的B为bmol,
2A(?)+B(?)?xC(g)
起始(mol) a a 0
转化(mol) 2b b xb
平衡(mol) a-2b a-b xb
根据题意
,解得x=2,故A错误;
B、根据图Ⅲ可知,反应正向进行,密度增大,而该反应是在恒容条件下,所以反应后气体的质量的增大,则A、B只有一种是气态,故B正确;
C、若A为气体,B为非气体,则反应前后气体的体积不变,压强对平衡移动没有影响,所以在恒容和恒压下可以达到等效平衡,因为两容器中起始量相等,所以平衡时M、N中C的物质的量相等,故C正确;
D、若A、B均为气体时,该反应是气体体积减小的反应,所以达到平衡时M中的压强大于N的压强,所以平衡时M中A的转化率大于N中A的转化率,故D正确;
故选A.
2A(?)+B(?)?xC(g)
起始(mol) a a 0
转化(mol) 2b b xb
平衡(mol) a-2b a-b xb
根据题意
|
B、根据图Ⅲ可知,反应正向进行,密度增大,而该反应是在恒容条件下,所以反应后气体的质量的增大,则A、B只有一种是气态,故B正确;
C、若A为气体,B为非气体,则反应前后气体的体积不变,压强对平衡移动没有影响,所以在恒容和恒压下可以达到等效平衡,因为两容器中起始量相等,所以平衡时M、N中C的物质的量相等,故C正确;
D、若A、B均为气体时,该反应是气体体积减小的反应,所以达到平衡时M中的压强大于N的压强,所以平衡时M中A的转化率大于N中A的转化率,故D正确;
故选A.
点评:本题主要考查影响平衡移动的因素,中等难度,解题关键在于区别恒温恒容和恒温恒压的条件.

练习册系列答案
相关题目
下列反应属于取代反应的是( )
| A、甲醇→甲醛 |
| B、丙醛→丙酸 |
| C、苯酚→三溴苯酚 |
| D、丁醇→丁烯 |
COCl2(g)?CO(g)+Cl2(g)△H>0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是( )


| A、①表示随温度升高,平衡常数的变化 |
| B、②表示t1时刻加入催化剂,反应速率随时间的变化 |
| C、③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化 |
| D、④表示CO的体积分数随充入Cl2量的变化 |
在电解水时,为了增强导电性,加入的电解质最好选用( )
| A、HCl |
| B、CuCl2 |
| C、Na2SO4 |
| D、CuSO4 |
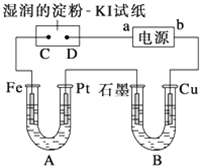 电解装置如图所示.图中B装置盛1L2mol?L-1的Na2SO4溶液,A装置中盛1L2mol?L-1 AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答:
电解装置如图所示.图中B装置盛1L2mol?L-1的Na2SO4溶液,A装置中盛1L2mol?L-1 AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答: