题目内容
下列说法正确的是
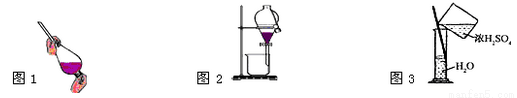
A. 萃取操作时,振荡过程中需要放气,放气是通过打开分液漏斗上口的玻璃塞进行的
B. 可以采用蒸发浓缩、冷却结晶的方法从硝酸钾溶液中获得硝酸钾晶体
C. 将乙醇与水分离,如图1、图2操作
D. 稀释浓H2SO4,如图3操作
练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
15.现有M、X、A、E4种元素的单质,能发生以下反应
①在水溶液中,M+X2+═M2++X
②A+2H2O(冷)═A(OH)2+H2↑
③X、E相连浸入稀H2SO4中,电极反应为:X-2e-═X2+,2H++2e-═H2↑
判断它们的还原性由强到弱的顺序是( )
①在水溶液中,M+X2+═M2++X
②A+2H2O(冷)═A(OH)2+H2↑
③X、E相连浸入稀H2SO4中,电极反应为:X-2e-═X2+,2H++2e-═H2↑
判断它们的还原性由强到弱的顺序是( )
| A. | M、X、A、E | B. | A、M、X、E | C. | M、X、E、A | D. | E、A、M |