题目内容
8g含有杂质的过氧化钠样品与水反应(杂质不溶于水,也不与水反应),收集到1.12L氧气(标准状况).则(1)过氧化钠与水反应的化学方程式是
(2)样品中过氧化钠的物质的量为 其质量为 .
【答案】分析:(1)过氧化钠可以和水之间发生反应生成氢氧化钠和氧气;
(2)根据过氧化钠和水之间的反应方程式进行计算即可.
解答:解:(1)过氧化钠可以和水之间发生反应生成氢氧化钠和氧气,方程式为:2Na2O2 +2H2O═4NaOH+O2↑,故答案为:2Na2O2 +2H2O═4NaOH+O2↑;
(2)根据过氧化钠和水之间的反应方程式2Na2O2 +2H2O═4NaOH+O2↑,
设生成1.12L的氢气消耗过氧化钠的物质的量是n,
2Na2O2 +2H2O═4NaOH+O2↑
2 1
n
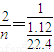 解得n=0.1mol,所以质量是0.1mol×78g/mol=7.8g
解得n=0.1mol,所以质量是0.1mol×78g/mol=7.8g
故答案为:0.1mol;7.8g.
点评:本题考查过氧化钠和水之间的反应以及根据化学方程式进行计算知识,注意知识的应用是关键,难度不大.
(2)根据过氧化钠和水之间的反应方程式进行计算即可.
解答:解:(1)过氧化钠可以和水之间发生反应生成氢氧化钠和氧气,方程式为:2Na2O2 +2H2O═4NaOH+O2↑,故答案为:2Na2O2 +2H2O═4NaOH+O2↑;
(2)根据过氧化钠和水之间的反应方程式2Na2O2 +2H2O═4NaOH+O2↑,
设生成1.12L的氢气消耗过氧化钠的物质的量是n,
2Na2O2 +2H2O═4NaOH+O2↑
2 1
n

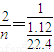 解得n=0.1mol,所以质量是0.1mol×78g/mol=7.8g
解得n=0.1mol,所以质量是0.1mol×78g/mol=7.8g故答案为:0.1mol;7.8g.
点评:本题考查过氧化钠和水之间的反应以及根据化学方程式进行计算知识,注意知识的应用是关键,难度不大.

练习册系列答案
相关题目