题目内容
在500mL1mol?L-1的CuSO4溶液中,阳极为100gCu片,阴极为100gZn片,通电一段时间后,立即取出电极,测得锌片质量增加到106.4g,此时剩余溶液中CuSO4的物质的量浓度为( )
分析:在500mL1mol?L-1的CuSO4溶液中,阳极为100gCu片,阴极为100gZn片,电解时阳极铜离子失去电子,阴极锌片上铜离子得到电子生成金属铜,相当于在锌片上镀铜,据此进行分析.
解答:解:由于阳极是铜,阴极是锌片,通电后,阳极铜失去电子生成铜离子、阴极溶液中的铜离子得到电子生成铜,相当于在锌片上镀铜,溶液中的硫酸铜浓度没有发生变化,所以仍然是500mL1mol?L-1的CuSO4溶液,
故选:C.
故选:C.
点评:本题考查了电解原理,注意进行电镀时,溶液中的溶质浓度不变,理解电镀原理是解题关键,本题难度中等.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
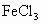 溶液中加入铁粉,完全反应后,除去多余的铁粉,加入足量的NaOH溶液,搅拌充分反应,所得沉淀的物质的量是
溶液中加入铁粉,完全反应后,除去多余的铁粉,加入足量的NaOH溶液,搅拌充分反应,所得沉淀的物质的量是