题目内容
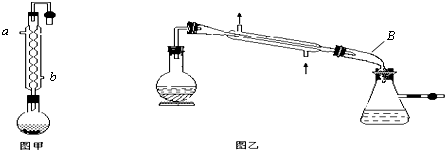
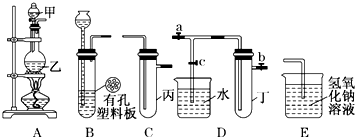
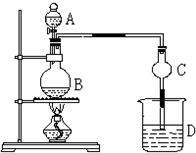 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液.(已知:无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH)请回答下列问题:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液.(已知:无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH)请回答下列问题:(1)浓硫酸的作用:
(2)球形干燥管C的作用是
(3)若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)
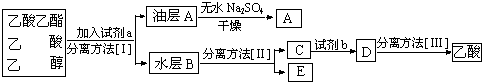
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出
考点:乙酸乙酯的制取
专题:实验题
分析:(1)乙酸与乙醇在浓硫酸作催化剂、加热的条件下发生酯化反应生成乙酸乙酯,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水;
(2)圆底烧瓶受热不均,球形干燥管的管口伸入液面下可能发生倒吸,同时起冷凝作用;
(3)醇与乙酸都易挥发,制备的乙酸乙酯含有乙醇与乙酸,通常用饱和碳酸钠溶液吸收乙酸乙酯,反应掉挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,故D中的溶液为饱和的碳酸钠溶液,碳酸根水解,溶液呈碱性,反应后溶液分层,上层无色油体液体,由于碳酸钠与乙酸反应,故下层溶液颜色变;
(4)用氯化钙除去少量乙醇和水,然后加入无水硫酸钠蒸馏出乙酸乙酯.
(2)圆底烧瓶受热不均,球形干燥管的管口伸入液面下可能发生倒吸,同时起冷凝作用;
(3)醇与乙酸都易挥发,制备的乙酸乙酯含有乙醇与乙酸,通常用饱和碳酸钠溶液吸收乙酸乙酯,反应掉挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,故D中的溶液为饱和的碳酸钠溶液,碳酸根水解,溶液呈碱性,反应后溶液分层,上层无色油体液体,由于碳酸钠与乙酸反应,故下层溶液颜色变;
(4)用氯化钙除去少量乙醇和水,然后加入无水硫酸钠蒸馏出乙酸乙酯.
解答:
解:(1)酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,由于反应加入的是乙酸钠,故浓硫酸还制乙酸的作用,故浓硫酸的作用为制乙酸、催化剂、吸水剂;
羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,其它基团相互结合生成酯,同时该反应可逆,反应的化学方程式为:CH3COOH+CH3CH218OH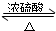 CH3CO18OC2H5+H2O,
CH3CO18OC2H5+H2O,
故答案为:催化剂、脱水剂;CH3COOH+CH3CH218OH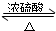 CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O;
(2)圆底烧瓶受热不均,球形干燥管的管口伸入液面下可能发生倒吸,球形干燥管体积大,可以防止倒吸,同时起冷凝作用,
故答案为:防止倒吸、冷凝;
(3)碳酸根离子水解:CO32-+H2O?HCO3-+OH-,溶液呈碱性,加入几滴酚酞,溶液呈红色;
碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,乙酸和碳酸钠反应而使溶液红色变浅,
故答案为:CO32-+H2O?HCO3-+OH-;溶液分层,上层无色油体液体,下层溶液颜色变浅;
(4)加入无水氯化钙除去少量乙醇和水,然后再加入无水硫酸钠进行蒸馏,从而分离出乙酸乙酯,故答案为:乙醇和水.
羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,其它基团相互结合生成酯,同时该反应可逆,反应的化学方程式为:CH3COOH+CH3CH218OH
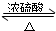 CH3CO18OC2H5+H2O,
CH3CO18OC2H5+H2O,故答案为:催化剂、脱水剂;CH3COOH+CH3CH218OH
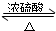 CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O;(2)圆底烧瓶受热不均,球形干燥管的管口伸入液面下可能发生倒吸,球形干燥管体积大,可以防止倒吸,同时起冷凝作用,
故答案为:防止倒吸、冷凝;
(3)碳酸根离子水解:CO32-+H2O?HCO3-+OH-,溶液呈碱性,加入几滴酚酞,溶液呈红色;
碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,乙酸和碳酸钠反应而使溶液红色变浅,
故答案为:CO32-+H2O?HCO3-+OH-;溶液分层,上层无色油体液体,下层溶液颜色变浅;
(4)加入无水氯化钙除去少量乙醇和水,然后再加入无水硫酸钠进行蒸馏,从而分离出乙酸乙酯,故答案为:乙醇和水.
点评:本题考查乙酸乙酯的制备与实验改进,题目难度中等,注意掌握乙酸乙酯的制取原理及装置选择,明确反应过程中浓硫酸、饱和碳酸钠溶液的作用,试题有利于提高学生的分析、理解能力及化学实验能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
能正确表示下列反应的离子方程式是( )
| A、醋酸钠的水解反应:CH3COO-+H3O+?CH3COOH+H2O |
| B、稀H2SO4与足量Ba(OH)2溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C、Fe(OH)3沉淀中加入足量HI:Fe(OH)3+3H+=Fe3++3H2O |
| D、AlCl3溶液中与过量氨水混合:Al3++3NH3?H2O=3NH4++Al(OH)3↓ |
下列叙述正确的是( )
A、
| ||||
B、
| ||||
| C、Na和K属于ⅠA族元素,Na的金属性比K强 | ||||
| D、Cl和Br属于VⅡA族元素,两原子核外电子数之差为8 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )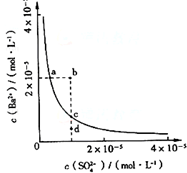

| A、加入Na2SO4可以使溶液由a点变到b点 |
| B、通过蒸发可以使溶液由d点变到c点 |
| C、a、b、c、d点溶液中Kw相等 |
| D、a点对应的Ksp大于c点对应的Ksp |
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,测得0到10秒内,c(H2)减小了0.75mol?L-1,下列说法正确的是( )
| A、10到15秒内c(NH3) 增加量等于0.25mol?L-1 |
| B、10秒内氨气的平均反应速率为0.025mol?L-1?s-1 |
| C、达平衡后,分离出少量NH3,v正增大 |
| D、该反应的逆反应的活化能不小于92.2kJ?mol-1 |
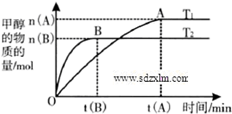 到2013午云南已连续4年干旱,专家认为云南和其他城市一样受到全球变暖的气候变化影响.CO2等温室气体是导致全球变暖的主要原因,控制和治理CO2是解决温室效应的有效途径.
到2013午云南已连续4年干旱,专家认为云南和其他城市一样受到全球变暖的气候变化影响.CO2等温室气体是导致全球变暖的主要原因,控制和治理CO2是解决温室效应的有效途径.