题目内容
14.某有机物的结构简式如下:HO-CH2-CH=CH-CH=CH-CH2-COOH(1)该有机物含有的官能团的名称是碳碳双键、羟基和羧基.
(2)验证该有机物中含有“-COOH”,常采用的试剂是紫色石蕊试液,产生的现象为变红(或NaHCO3、Na2CO3溶液,有气体生成).
(3)对该有有机物的性质描述正确的是AD.
A.金属Na反应放出H2 B.与Cl2只能发生加成反应,不能发生取代反应
C.1mol该有机物可与2mol NaOH反应 D.一定条件能与H2发生加成反应
(4)1mol该有机物完全与溴水发生加成反应时,需要Br22mol.
(5)请选择适当试剂,检验该有机物分子中含有醇羟基,并写出试验方法和现象:取少量该有机物加入适量溴水,使碳碳双键完全反应,再加入少量酸性高锰酸钾溶液,溶液褪色则说明含醇羟基.
分析 (1)该有机物含有的官能团的名称是碳碳双键、羟基和羧基;
(2)酸能使紫色石蕊试液变红色,该羧基能和碳酸钠、碳酸氢钠反应生成气体;
(3)该物质中含有碳碳双键、羟基、羧基,具有烯烃、醇和羧酸性质;
(4)1mol该有机物完全与溴水发生加成反应时,有几摩尔碳碳双键,最多需要Br2几摩尔;
(5)醇羟基的检验要根据醇羟基的性质来进行,避开双键和羧基的干扰.
解答 解:(1)该有机物含有的官能团的名称是碳碳双键、羟基和羧基,故答案为:碳碳双键、羟基和羧基;
(2)含有-COOH的羧酸具有酸的通性:可以使紫色石蕊试液变红,和碳酸钠、碳酸氢钠反应生成二氧化碳,故答案为:紫色石蕊试液;变红(或NaHCO3、Na2CO3溶液,有气体生成);
(3)A.羧基和羟基都能与金属Na反应放出氢气,故正确;
B.碳碳双键与Cl2能发生加成反应,连接羧基的亚甲基能发生取代反应,故错误;
C.只有羧基能和NaOH反应,则1mol该有机物可与1mol NaOH反应,故错误;
D.碳碳双键在一定条件能与H2发生加成反应,故正确;
故选AD;
(4)1mol该有机物完全与溴水发生加成反应时,有几摩尔碳碳双键,最多需要Br2几摩尔,该物质中含有2个碳碳双键,所以1mol该有机物完全与溴水发生加成反应时,需要Br2 2mol,故答案为:2;
(5)醇羟基的检验要根据醇羟基的性质:和金属反应放氢气、能使酸性高锰酸钾溶液褪色,但是碳碳双键也能使酸性高锰酸钾溶液褪色,所以要避开双键的干扰,
故答案为:取少量该有机物加入适量溴水,使碳碳双键完全反应,再加入少量酸性高锰酸钾溶液,溶液褪色则说明含醇羟基.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃、醇和羧酸性质,易错点是醇羟基的检验,要排除其它官能团的干扰,题目难度不大.

| A | B | |
| 实验 方案 | 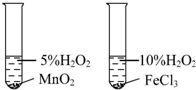 | 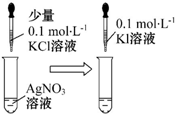 |
| 实验 目的 | 比较不同催化剂对同一反应速率的影响 | 证明:Ksp(AgCl)>Ksp(AgI) |
| C | D | |
| 实验 方案 | 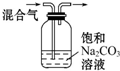 | 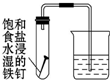 |
| 实验 目的 | 除去CO2气体中混有的SO2 | 证明铁钉生锈过程中有氧气参与反应 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 环己醇分子中所有的原子可能共平面 | |
| B. | 按系统命名法,(CH3CH2)2CHCH3化合物的名称是3-乙基丁烷 | |
| C. | 芳香化合物A(C8H8O3)分子中含有酯基和醚键两种含氧官能团,A可能的同分异构体有4种 | |
| D. | 在一定条件下,1.0 mol的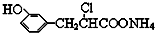 最多能与含4.0 mol NaOH的溶液完全反应 最多能与含4.0 mol NaOH的溶液完全反应 |
实验流程如下:
金坷垃$→_{加热}^{辅助试剂}$(NH4)2SO4溶液$→_{吹出}^{NaOH}$NH3$→_{吸收}^{H_{3}BO_{3}}$(NH4)2B4O7溶液→用标准盐酸滴定
步骤:①取10.00g“金坷垃”尿素[CO(NH2)2]化肥溶于水,定容至100mL;
②在烧杯中加入10.00mL步骤①中得到的金坷垃水溶液和辅助试剂,加热充分反应;
③将反应液转移到大试管中;
④按如图2装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
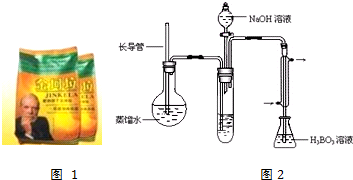
⑤取下锥形瓶,滴加指示剂,用0.2500mol•L-1盐酸标准液滴定;
⑥重复实验操作.
数据记录如表1:
表1
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.90 |
| 3 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | x |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl.
(2)步骤③的实验装置中需要加热的仪器是圆底烧瓶(填仪器名称),长导管的作用是作为安全管,防止装置中压力过大而发生危险;防止冷却时发生倒吸.
(3)编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸,理由是空白、等量对照以消除其他试剂、实验操作等因素引起的误差.
(4)通过计算可得“金坷垃”化肥中的氮含量为117.67-3.5x克/每千克化肥(用含x的代数式表示,要求化简).我国农业用尿素的标准为:
表2
| 级别 | 优等品 | 一等品 | 合格品 |
| 总尿素含量%≥ | 46.4 | 46.2 | 46.0 |
| A. | 向FeI2溶液中通入少量氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 将少量CO2通入NH3•H2O中:CO2+2NH3•H2O═(NH4)2CO3+H2O | |
| C. | 将少量SO2通入NH3•H2O中:SO2+2NH3•H2O═(NH4)2SO3+H2O | |
| D. | 将AlCl3与等量Na2CO3溶液混合:3H2O+Al3++CO32-═HCO3-+Al(OH)3+2H+ |

 现有一瓶标签受到腐蚀(如图所示)的无色溶液,已知该溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠、硫化钠中的一种,为确定溶液的成分,同学们进行了如下探究:
现有一瓶标签受到腐蚀(如图所示)的无色溶液,已知该溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠、硫化钠中的一种,为确定溶液的成分,同学们进行了如下探究: (1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.
(1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.