题目内容
18.下列离子方程式错误的是( )| A. | 碳酸氢镁与氢氧化钠反应:Mg2++2HCO3-+2OH-═MgCO3↓+2H2O | |
| B. | 溴化亚铁溶液中通入过量的氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| C. | 碳酸钙中滴入醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O | |
| D. | 偏铝酸钠溶液中通入过量的CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
分析 A.离子方程式两边电荷不守恒;
B.氯气过量,亚铁离子和溴离子都完全被氧化;
C.碳酸钙和醋酸都需要保留化学式,二者反应生成醋酸钙、二氧化碳气体和水;
D.二氧化碳过量,反应生成氢氧化铝沉淀和碳酸氢根离子.
解答 解:A.碳酸氢镁与氢氧化钠反应时,若氢氧化钠过量,反应生成氢氧化镁沉淀、碳酸钠和水,反应的离子方程式为:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2H2O+CO32-,故A错误;
B.溴化亚铁溶液中通入过量的氯气,反应生成氯化铁、溴单质,反应的离子方程式为:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故B正确;
C.碳酸钙中滴入醋酸,二者反应的离子方程式为:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O,故C正确;
D.偏铝酸钠溶液中通入过量的CO2,反应的离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故D正确;
故选A.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
8.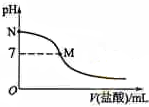 298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
 298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )| A. | 该滴定过程应该选择石蕊作为指示剂 | |
| B. | M点对应的盐酸体积为20.0 mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
9. (1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
(1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
对比实验1和3,表明影响化学反应速率的因素是浓度的大小;此外,该实验表明影响化学反应速率的因素还有固体表面积(说出一种即可).
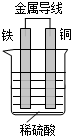
(2)用如图原电池装置可加快铁与稀硫酸反应的速率,此装置可以把化学能转化为电能,其中铁作负极(填“负极”或“正极”).
(3)举出生活中你熟悉的一种电池普通干电池,手机充电电池,铅蓄电池.
 (1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
(1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:| 实验序号 | 金属质量 /g | 金属状态 | c(H2SO4) /mol•L-1 | V(H2SO4) /mL | 反应前溶液温度/℃ | 金属消失的时间/s |
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 50 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 |
(2)用如图原电池装置可加快铁与稀硫酸反应的速率,此装置可以把化学能转化为电能,其中铁作负极(填“负极”或“正极”).
(3)举出生活中你熟悉的一种电池普通干电池,手机充电电池,铅蓄电池.
6.在20℃时,某气态烃与氧气混合装入密闭容器中,点燃爆炸后,又恢复到20℃.此时容器内气体的压强为反应前的一半,经NaOH溶液吸收后,容器内几乎真空.此烃的化学式可能是( )
| A. | CH4 | B. | C3H4 | C. | C2H4 | D. | C4H8 |
10.反应N2(g)+3H2(g)?2NH3(g)在密闭容器中进行.下列关于该反应的说法中错误的是( )
| A. | 升高温度能加快反应速率 | |
| B. | 减小压强会减慢反应速宇. | |
| C. | N2和H2能100%转化为NH3 | |
| D. | 反应达到平衡状态时,正、逆反应的速率都为0 |
7.对比甲烷和乙烯的燃烧反应,下列叙述中正确的是( )
| A. | 二者燃烧时现象完全相同 | |
| B. | 点燃前都不用验纯 | |
| C. | 甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮并伴有黑烟 | |
| D. | 二者燃烧时都有黑烟生成 |
8.某溶液中含有CH3COO-、SO42-、SO32-、HCO3-、CO32-等五种离子.将过量的Na2O2固体加入其中后,仍能大量存在的离子是( )
| A. | CH3COO-、SO42-、HCO3- | B. | SO42-、SO32-、CO32- | ||
| C. | SO32-、HCO3- | D. | CH3COO-、SO42-、CO32- |