题目内容
相同状况下,2.24LCH4和C2H4的混合气体完全燃烧需要 5.6L氧气,则混合气体中乙烷的体积分数为
- A.95%
- B.50%
- C.45%
- D.25%
B
分析:根据反应的方程式,列方程组计算.反应的方程式分别为:CH4+2O2 CO2+2H2O,C2H4+3O2
CO2+2H2O,C2H4+3O2 2CO2+2H2O.
2CO2+2H2O.
解答:设混合气体中含有xLCH4,yLC2H4,
CH4+2O2 CO2+2H2O
CO2+2H2O
xL 2xL
C2H4+3O2 2CO2+2H2O
2CO2+2H2O
yL 3yL
则有: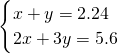 ,
,
解之得: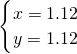 ,
,
则混合气体中乙烷的体积分数为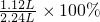 =50%,
=50%,
故选B.
点评:本题考查混合物的计算,题目难度不大,注意有机物燃烧的化学方程式的书写,注意耗氧量的有关计算.
分析:根据反应的方程式,列方程组计算.反应的方程式分别为:CH4+2O2
 CO2+2H2O,C2H4+3O2
CO2+2H2O,C2H4+3O2 2CO2+2H2O.
2CO2+2H2O.解答:设混合气体中含有xLCH4,yLC2H4,
CH4+2O2
 CO2+2H2O
CO2+2H2OxL 2xL
C2H4+3O2
 2CO2+2H2O
2CO2+2H2OyL 3yL
则有:
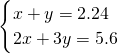 ,
,解之得:
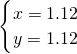 ,
,则混合气体中乙烷的体积分数为
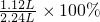 =50%,
=50%,故选B.
点评:本题考查混合物的计算,题目难度不大,注意有机物燃烧的化学方程式的书写,注意耗氧量的有关计算.

练习册系列答案
相关题目