题目内容
8.按电子排布,可把周期表里的元素划分成5个区,以下元素属于p区的是( )| A. | Fe | B. | S | C. | Mg | D. | Cu |
分析 电子最后填入的能级是p能级的元素属于p区元素,p区元素的外围电子排布为ns2npx(注意氦元素除外);电子最后填入的能级是s能级的元素属于s区元素,电子最后填入的能级是d能级的元素属于d区元素,电子最后填入的能级是p能级的元素属于P区元素,ds区包括ⅠB族(11列)、ⅡB族(12列),可以理解为先填d能级后填s能级而得名,据此进解答.
解答 解:A.Fe的外围电子排布为3d64s2,属于d区元素,故A错误;
B.S的外围电子排布为3s23p4,属于p区元素,故B正确;
C.Mg的外围电子排布为3s2,属于s区元素,故C错误;
D.Cu的外围电子排布为3d104s1,属于ds区元素,故D错误;
故选B.
点评 本题考查元素原子结构与位置关系,为高频考点,把握元素的电子排布及最后填充的电子为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
19.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 2NA个二氧化碳分子的质量为44g | |
| B. | 2.4g金属镁与足量盐酸完全反应,失电子总数为0.2NA | |
| C. | 0.1mol/LNaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| D. | 17g氨气中所含原子数为NA |
16.下列四种固体物质中,既存在离子键又存在共价键的是( )
| A. | NH4Cl | B. | K2S | C. | MgCl2 | D. | SO3 |
3.将钠、镁、铝各0.3mol 分别放入100mL1mol/L 的盐酸中,同温同压下产生的气体体积比是( )
| A. | 1:1:1 | B. | 3:1:1 | C. | 1:2:3 | D. | 6:3:2 |
13.室温下,下列溶液的说法不正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
| pH | 11 | 11 | 3 | 3 |
| A. | 水的电离程度:①=②=③=④ | |
| B. | 分别加水稀释10倍,溶液的pH:①>②>③>④ | |
| C. | ①、③两溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | V1L②溶液与V2 L③溶液混合,若混合溶液pH=4,则V1:V2=9:11(忽略溶液体积变化) |
20.元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
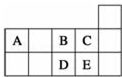

| A. | D在过量的B中燃烧的主要产物为DB3 | |
| B. | C的氢化物的水溶液酸性比E的强 | |
| C. | D与B形成的阴离子可能有DB32-、DB42- | |
| D. | E单质由于分子间形成了氢键,所以很容易液化 |
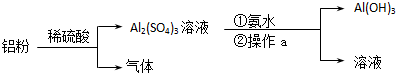
 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )