题目内容
现有下列物质:①HNO3 ②冰醋酸 ③氨水 ④Al(OH)3 ⑤NaHCO3(s) ⑥Cu ⑦氯水 ⑧CaCO3⑨H2CO3⑩盐酸
(1)上述物质中属于强电解质的有 ,属于弱电解质的有 .
(2)写出下列物质的电离方程式:
② ;④ ;
⑤ ;⑨ .
(1)上述物质中属于强电解质的有
(2)写出下列物质的电离方程式:
②
⑤
考点:强电解质和弱电解质的概念,电离方程式的书写
专题:
分析:(1)电解质:在水溶液中或熔融状态下能够导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质;
(2)强电解质的电离不可逆,用“═”,弱电解质的电离可逆,用“?”,原子团不能拆开写.
在水溶液中完全电离的是强电解质;部分电离的是弱电解质;
(2)强电解质的电离不可逆,用“═”,弱电解质的电离可逆,用“?”,原子团不能拆开写.
解答:
解:(1)①硝酸在水溶液中完全电离,是强电解质;
②CH3COOH在水溶液中部分电离,是弱电解质;
③氨水是混合物,既不是电解质也不是非电解质;
④氢氧化铝在水溶液中部分电离,是弱电解质;
⑤NaHCO3在水溶液中完全电离,是强电解质;
⑥铜是单质,既不是电解质也不是非电解质;
⑦氯水是混合物,既不是电解质也不是非电解质;
⑧碳酸钙溶于水的部分全部电离,属于强电解质;
⑨H2CO3在水溶液中部分电离,属于弱电解质;
⑩盐酸是混合物,既不是电解质也不是非电解质;
故属于强电解质的是:①⑤⑧,属于弱电解质的是②④⑨;
故答案为:①⑤⑧;②④⑨;
(2)醋酸、碳酸、氢氧化铝为弱电解质,电离方程式用“?”号,碳酸氢钠为强电解质,电离方程式用“=”号,
CH3COOH?CH3COO-+H+;H2O+AlO2-+H+?Al(OH)3?Al3++3OH-;NaHCO3=Na++HCO3-;H2CO3?H++HCO3-,故答案为:
CH3COOH?CH3COO-+H+;H2O+AlO2-+H+?Al(OH)3?Al3++3OH-;NaHCO3=Na++HCO3-;H2CO3?H++HCO3-.
②CH3COOH在水溶液中部分电离,是弱电解质;
③氨水是混合物,既不是电解质也不是非电解质;
④氢氧化铝在水溶液中部分电离,是弱电解质;
⑤NaHCO3在水溶液中完全电离,是强电解质;
⑥铜是单质,既不是电解质也不是非电解质;
⑦氯水是混合物,既不是电解质也不是非电解质;
⑧碳酸钙溶于水的部分全部电离,属于强电解质;
⑨H2CO3在水溶液中部分电离,属于弱电解质;
⑩盐酸是混合物,既不是电解质也不是非电解质;
故属于强电解质的是:①⑤⑧,属于弱电解质的是②④⑨;
故答案为:①⑤⑧;②④⑨;
(2)醋酸、碳酸、氢氧化铝为弱电解质,电离方程式用“?”号,碳酸氢钠为强电解质,电离方程式用“=”号,
CH3COOH?CH3COO-+H+;H2O+AlO2-+H+?Al(OH)3?Al3++3OH-;NaHCO3=Na++HCO3-;H2CO3?H++HCO3-,故答案为:
CH3COOH?CH3COO-+H+;H2O+AlO2-+H+?Al(OH)3?Al3++3OH-;NaHCO3=Na++HCO3-;H2CO3?H++HCO3-.
点评:本题考查强弱电解质、非电解质概念的辨析及电离方程式的书写,较基础,注意电离方程式的书写原则.

练习册系列答案
相关题目
下列关于氯气的叙述正确的是( )
| A、氢气在氯气中燃烧产生苍白色火焰 |
| B、氯气的水溶液用于漂白,是利用氯气的强氧化性 |
| C、铁丝在氯气中燃烧生成FeCl2 |
| D、当有大量氯气逸到空气中时,可用浸有NaOH溶液的毛巾捂住鼻子 |
下列叙述正确的是( )
| A、水的摩尔质量是18g |
| B、标准状况下,1.8L CCl4和1.8L NH3所含分子个数相同 |
| C、在标准状况下,1mol任何物质的体积都约为22.4L |
| D、将73gHCl溶于水中配成1L溶液,所得溶液物质的量浓度是2mol/L |
苹果酸的结构简式为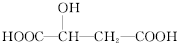 ,下列说法正确的是( )
,下列说法正确的是( )
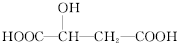 ,下列说法正确的是( )
,下列说法正确的是( )A、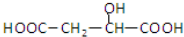 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
| B、1 mol苹果酸可与3 mol NaOH发生中和反应 |
| C、1 mol苹果酸与足量金属Na反应生成1 mol H2 |
| D、四联苯的一氯代物有5种 |
