题目内容
13.有A、B、C、D四种元素,A、D是相邻的短周期元素,它们的核外电子数之和是33,B、C同主族,核电荷数之和是22,C的最高价态有两种含氧酸,又知D元素可形成氧化物DOm和DOn,其相对分子质量只差为16,DOm中含氧60%,DOn中含氧50%,试确定A、B、C、D各是什么元素.分析 有A、B、C、D四种元素,A、D是相邻的短周期元素,它们的核外电子数之和是33,分别为S、Cl元素,D元素可形成氧化物DOm和DOn,其相对分子质量只差为16,DOm中含氧60%,DOn中含氧50%,则D为S元素、A为Cl元素;B、C同主族,核电荷数之和是22,C的最高价态有两种含氧酸,B为N元素、C为P元素.
解答 解:有A、B、C、D四种元素,A、D是相邻的短周期元素,它们的核外电子数之和是33,分别为S、Cl元素,D元素可形成氧化物DOm和DOn,其相对分子质量只差为16,SO3中含氧60%,SO2中含氧50%,则D为S元素、A为Cl元素;B、C同主族,核电荷数之和是22,C的最高价态有两种含氧酸,B为N元素、C为P元素,C形成2种酸为HPO3、H3PO4,
答:A为氯元素,B为氮元素,C为磷元素,D为硫元素.
点评 本题考查元素推断,关键是熟练掌握短周期元素以及元素化合物组成,C元素最高价价态形成的两种酸为知识盲点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列做法不正确的是( )
| A. | 二氧化硫用作食品防腐剂 | |
| B. | 明矾用于水的净化 | |
| C. | 盛放氢氧化钠溶液时,使用带橡皮塞的磨口瓶 | |
| D. | 在常温下用铝制贮罐贮运浓硫酸 |
4.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表.J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
(1)M的离子结构示意图为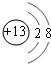 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族.
(2)J和氢组成10电子的化合物,其分子式为CH4.
(3)M和T的最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+3HClO4═Al(ClO4)3+3H2O.
| J | ||||
| R |
 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族.(2)J和氢组成10电子的化合物,其分子式为CH4.
(3)M和T的最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+3HClO4═Al(ClO4)3+3H2O.
1.根据表中部分短周期元素的原子半径和主要化合价信息判断,以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 单质与同浓度稀盐酸反应的速率为L<M | |
| B. | R与T形成的化合物一定能使品红溶液褪色 | |
| C. | 氢化物的稳定性为:H2T>H2R | |
| D. | 当单质L着火时,可用CO2灭火 |
18.下列物质的比较正确的是( )
| A. | 酸性:HIO4>HBrO4>HClO4 | B. | 原子半径:Na>Cl>S | ||
| C. | 碱性:KOH>NaOH>LiOH | D. | 金属性:Na>Al>Mg |
5.已知可逆反应:N2(g)+3H2(g)?2NH3(g),这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下列关于此反应的说法中错误的是( )
| A. | 升高反应体系的温度,可使反应速率变大 | |
| B. | 该反应中N2不可能100%转化为NH3 | |
| C. | 该反应达到平衡状态时,N2、H2和NH3三者的浓度一定相等 | |
| D. | 为了提高H2的转化率,可适当提高N2的浓度 |
 ;过氧化钠
;过氧化钠 .
.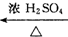 A(C4H8O3)$→_{△}^{浓H_{2}SO_{4}}$乙,甲、乙的分子式都为C4H6O2,甲能使溴的四氯化碳溶液褪色,乙为五元环状化合物,则甲不能发生的反应类型有( )
A(C4H8O3)$→_{△}^{浓H_{2}SO_{4}}$乙,甲、乙的分子式都为C4H6O2,甲能使溴的四氯化碳溶液褪色,乙为五元环状化合物,则甲不能发生的反应类型有( )