题目内容
硫酸亚铁晶体(FeSO4?7H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量.实验步骤如下:
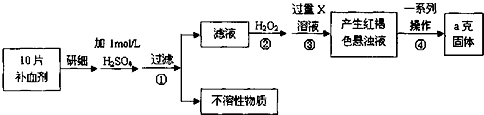
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是 ,
该过程涉及的离子反应为: 、 .
(2)若向步骤①滤液中加入足量NaOH溶液,则出现白色沉淀、迅速变为灰绿色、最后变为红褐色,原因是(用化学方程式解释) .
(3)步骤②加入过量H2O2的目的: .
(4)步骤③中反应的离子方程式: .
(5)步骤④中一系列处理的操作步骤:过滤、洗涤、灼烧、冷却、称量.若实验无损耗,则每片补血剂含铁元素的质量 g.(用含a的式子表示)

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是
该过程涉及的离子反应为:
(2)若向步骤①滤液中加入足量NaOH溶液,则出现白色沉淀、迅速变为灰绿色、最后变为红褐色,原因是(用化学方程式解释)
(3)步骤②加入过量H2O2的目的:
(4)步骤③中反应的离子方程式:
(5)步骤④中一系列处理的操作步骤:过滤、洗涤、灼烧、冷却、称量.若实验无损耗,则每片补血剂含铁元素的质量
考点:物质分离和提纯的方法和基本操作综合应用,探究物质的组成或测量物质的含量
专题:实验设计题
分析:由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量.
(1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,可以加入氧化剂将Fe2+氧化为Fe3+.检验Fe2+可以先滴加KSCN溶液,溶液不变色,再滴加氯水或双氧水,溶液变为血红色,说明含有Fe2+;
(2)步骤①滤液中含有Fe2+,加入氢氧化钠生成Fe(OH)2,Fe(OH)2不稳定,可被氧化生成Fe(OH)3;
(3)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,由流程图可知,加入H2O2是将Fe2+氧化为Fe3+;
(4)步骤③是将Fe3+转化为氢氧化铁沉淀;
(5)根据铁元素守恒可知ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,据此计算.
(1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,可以加入氧化剂将Fe2+氧化为Fe3+.检验Fe2+可以先滴加KSCN溶液,溶液不变色,再滴加氯水或双氧水,溶液变为血红色,说明含有Fe2+;
(2)步骤①滤液中含有Fe2+,加入氢氧化钠生成Fe(OH)2,Fe(OH)2不稳定,可被氧化生成Fe(OH)3;
(3)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,由流程图可知,加入H2O2是将Fe2+氧化为Fe3+;
(4)步骤③是将Fe3+转化为氢氧化铁沉淀;
(5)根据铁元素守恒可知ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,据此计算.
解答:
解:由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量.
(1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,可以加入氧化剂将Fe2+氧化为Fe3+,检验Fe2+可以先滴加KSCN溶液,溶液不变色,加入氯水或过氧化氢,发生2Fe2++Cl2═2Fe3++2Cl-,溶液变为血红色,发生Fe3++3SCN-═Fe(SCN)3,说明含有Fe2+.
故答案为:先加KSCN溶液,再加入氯水(或双氧水、稀硝酸);2Fe2++Cl2═2Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3;
(2)步骤①滤液中含有Fe2+,加入氢氧化钠生成Fe(OH)2,Fe(OH)2不稳定,可被氧化生成Fe(OH)3,发生4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,故答案为:将Fe2+氧化为Fe3+;
(4)步骤③是将Fe3+转化为氢氧化铁沉淀,反应离子方程式为Fe3++3OH-═Fe(OH)3↓或Fe3++3NH3.H2O═Fe(OH)3↓+3NH4+,
故答案为:Fe3++3OH-═Fe(OH)3↓或Fe3++3NH3.H2O═Fe(OH)3↓+3NH4+;
(5)ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,所以每片补血剂含铁元素的质量
=0.07ag,
故答案为:0.07a.
(1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,可以加入氧化剂将Fe2+氧化为Fe3+,检验Fe2+可以先滴加KSCN溶液,溶液不变色,加入氯水或过氧化氢,发生2Fe2++Cl2═2Fe3++2Cl-,溶液变为血红色,发生Fe3++3SCN-═Fe(SCN)3,说明含有Fe2+.
故答案为:先加KSCN溶液,再加入氯水(或双氧水、稀硝酸);2Fe2++Cl2═2Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3;
(2)步骤①滤液中含有Fe2+,加入氢氧化钠生成Fe(OH)2,Fe(OH)2不稳定,可被氧化生成Fe(OH)3,发生4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,故答案为:将Fe2+氧化为Fe3+;
(4)步骤③是将Fe3+转化为氢氧化铁沉淀,反应离子方程式为Fe3++3OH-═Fe(OH)3↓或Fe3++3NH3.H2O═Fe(OH)3↓+3NH4+,
故答案为:Fe3++3OH-═Fe(OH)3↓或Fe3++3NH3.H2O═Fe(OH)3↓+3NH4+;
(5)ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,所以每片补血剂含铁元素的质量
ag×
| ||
| 10 |
故答案为:0.07a.
点评:本题考查学生对实验原理与实验操作的理解、物质分离提纯、元素化合物性质、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

练习册系列答案
相关题目
有关物质与反应分类的下列说法中,正确的是( )
| A、硅酸钠是钠盐,也是硅酸盐 |
| B、碳酸钠使无色酚酞试液变红,属于碱 |
| C、CO2溶于水能导电,属电解质 |
| D、CO还原氧化铁获得铁,属于置换反应 |
将含有等体积NH3、CO2、NO的混合气体依次通过盛有浓H2SO4、Na2O2和Na2CO3溶液的装置,充分反应,最后得到的气体是( )
| A、CO2和NO |
| B、CO2 |
| C、NO |
| D、NO2 |