题目内容
其他条件不变,升高温度下列数据不一定增大的是( )
| A、水的离子积常数 |
| B、醋酸的电离平衡常数 |
| C、放热反应的正反应速率 |
| D、可逆反应的化学平衡常数 |
考点:水的电离,化学平衡常数的含义,化学反应速率的影响因素,弱电解质在水溶液中的电离平衡
专题:化学平衡专题
分析:A、水的电离过程是吸热的,升高温度促进水的电离;
B、醋酸的电离过程是吸热的,升温可促进醋酸的电离;
C、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快.这一点不要和化学平衡的移动混淆;
D、根据勒夏特列原理,对所有可逆反应升温平衡都向吸热的方向移动.可逆反应的正反应既有吸热反应也有放热反应,要区别对待.
B、醋酸的电离过程是吸热的,升温可促进醋酸的电离;
C、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快.这一点不要和化学平衡的移动混淆;
D、根据勒夏特列原理,对所有可逆反应升温平衡都向吸热的方向移动.可逆反应的正反应既有吸热反应也有放热反应,要区别对待.
解答:
解:A、水的电离过程是吸热的,升高温度促进水的电离,升高温度电离程度增大,水的离子积一定增大,故A错误;
B、醋酸的电离过程是吸热的,升温可促进醋酸的电离,使平衡向着电离的方向移动,醋酸的电离平衡常数一定增大,故B错误;
C、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快,故C错误;
D、若正反应为放热反应,升高温度平衡向逆反应移动,化学平衡常数减小,若正反应为吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故D正确.
故选:D.
B、醋酸的电离过程是吸热的,升温可促进醋酸的电离,使平衡向着电离的方向移动,醋酸的电离平衡常数一定增大,故B错误;
C、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快,故C错误;
D、若正反应为放热反应,升高温度平衡向逆反应移动,化学平衡常数减小,若正反应为吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故D正确.
故选:D.
点评:本题考查温度对水的离子积、电离平衡常数、反应速率以及化学平衡常数的影响,比较基础.注意温度对化学反应速率和化学平衡影响的区别,不要混淆.

练习册系列答案
相关题目
2007年度诺贝尔化学奖,授予致力于研究合成氨与催化剂表面积大小关系的德国科学家格哈德?埃特尔,表彰他在“固体表面化学过程”研究中作出的贡献.下列说法中正确的是( )
| A、工业生产中,合成氨采用压强越高,温度越低,越有利于提高经济效益 |
| B、增大催化剂的表面积,能加快合成氨的正反应速率、降低逆反应速率 |
| C、采用催化剂时,反应的活化能降低,使反应易达过渡态,故明显加快 |
| D、增大催化剂的表面积,能增大氨气的产率 |
下面离子方程式书写不正确的是( )
| A、消毒液与洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+═Cl2↑+H2O | ||||
B、用惰性电极电解AlCl3溶液会产生白色沉淀:2Al3++6Cl-+6H2O
| ||||
| C、在重铬酸钾溶液中滴入NaOH溶液,溶液变为黄色:Cr2O72-+2OH-═2CrO42-+H2O | ||||
| D、草酸使得酸性高锰酸钾溶液褪色:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O |
100mL 0.1mol?L-1的碳酸钠溶液所含碳酸钠的质量是( )
| A、10.6g | B、1.06g |
| C、0.53g | D、106g |
已知某气体的摩尔质量为Mg/mol,则b g该气体在标准状况下的体积(L)为( )
| A、22.4Mb | ||
B、
| ||
C、
| ||
| D、22.4b |
下列物质易溶于水的是( )
| A、硝酸钾 | B、氮气 |
| C、一氧化碳 | D、氯化银 |
下列烷烃在光照下与氯气反应,生成两种一氯代烃的是( )
| A、CH3CH2CH2CH2CH3 |
B、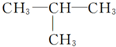 |
C、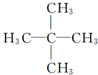 |
D、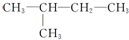 |
在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是( )
| A、范德华力、范德华力、范德华力 |
| B、范德华力、范德华力、共价键 |
| C、范德华力、共价键、共价键 |
| D、共价键、共价键、共价键 |
pH=4的盐酸和pH=4氯化铵溶液中,由水电离产生的氢离子浓度之比为( )
| A、1:1 |
| B、1:104 |
| C、1:106 |
| D、1:108 |