题目内容
13. 如图,B为常见金属或非金属单质,有下列转化关系.若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是( )
如图,B为常见金属或非金属单质,有下列转化关系.若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是( )| A. | CuCl2 | B. | AlCl3 | C. | H2O2 | D. | NaCl |
分析 可用作自来水消毒的气体C是Cl2,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,可知D是Na2O,E是Na2O2,则B是Na,A是NaCl;
解答 解:可用作自来水消毒的气体C是Cl2,由氧化物D转化为氧化物E时,增加氧的质量约是D物质总质量的25.8%,
可知D是Na2O,E是Na2O2,存在:$\frac{16}{62}$×100%=25.8%,其转化过程为:NaCl$\frac{\underline{\;通电\;}}{\;}$Na$\stackrel{O_{2}}{→}$Na2O$\stackrel{O_{2}}{→}$Na2O2,
则B是Na,A是NaCl,
故选D.
点评 本题考查无机物的推断,题目难度中等,注意根据物质的物理特性作为推断的突破口,把握物质的性质以及相互之间的转化关系.

练习册系列答案
相关题目
3.下列是元素周期表的短周期中的部分元素
(1)表中元素,原子半径最大的是Na,原子半径最小的是H.(不包括稀有气体元素.填空均用元素符号或化学式回答,下同)
(2)金属性最强的是Na;化学性质最不活泼的是Ne;最高正价和负价的绝对值相等的是C;氢化物水溶液呈碱性的是NH3.
(3)I和L最高价氧化物对应的水化物酸性较强的是HClO4,判断依据之一是HCl比H2S更稳定(或Cl2与H2化合比S与H2化和更容易).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | L |
(2)金属性最强的是Na;化学性质最不活泼的是Ne;最高正价和负价的绝对值相等的是C;氢化物水溶液呈碱性的是NH3.
(3)I和L最高价氧化物对应的水化物酸性较强的是HClO4,判断依据之一是HCl比H2S更稳定(或Cl2与H2化合比S与H2化和更容易).
4.在蒸发器中加热蒸干并灼烧(低于400℃)下列物质的溶液,可以得到该物质固体的是( )
| A. | CuCl2 | B. | 碳酸氢钾 | C. | 硫酸镁 | D. | 硝酸银 |
1.下列有关化学反应的描述中不正确的是( )
| A. | 一定条件下的可逆反应,反应物的转化率不可能达到100% | |
| B. | △H<0,△S>0的化学反应一定能自发进行 | |
| C. | 已知C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol | |
| D. | 同一反应中,△H的大小与化学反应中参加反应的物质的量无关 |
8.某化学反应中,设反应物的总能量为E1,生成物的总能量为E2.
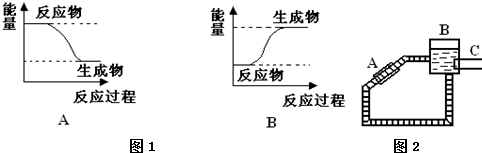
(1)若E1>E2,则该反应为放热(填“放热”或“吸热”)反应.该反应可用图1A(填“A”或“B”)表示.
(2)太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
其中最适宜作储能介质的一种盐是B(填字母).
A.CaCl2•6H2OB.Na2SO4•10H2O
C.Na2HPO4•12H2OD.Na2S2O3•5H2O
②图2是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.
根据对水的密度的认识,你估计在阳光照射下水将沿顺(填“顺”或“逆”)时针方向流动.

(1)若E1>E2,则该反应为放热(填“放热”或“吸热”)反应.该反应可用图1A(填“A”或“B”)表示.
(2)太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
| 盐 | 熔点/℃ | 熔化吸热/KJ•mol-1 | 参考价格/元•kg-1 |
| CaCl2•6H2O | 29.0 | 37.3 | 780~850 |
| Na2SO4•10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4•12H2O | 36.1 | 100.1 | 1600~2000 |
| Na2S2O3•5H2O | 48.5 | 49.7 | 1400~1800 |
A.CaCl2•6H2OB.Na2SO4•10H2O
C.Na2HPO4•12H2OD.Na2S2O3•5H2O
②图2是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.
根据对水的密度的认识,你估计在阳光照射下水将沿顺(填“顺”或“逆”)时针方向流动.
18.用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 1 L 0.1 mol•L-1的乙醇溶液中分子总数为0.1NA | |
| B. | 常温常压下,28 g乙烯含有的电子数为16NA | |
| C. | 44g乙酸乙酯和丁酸的混合物中共含有碳原子数为2 NA | |
| D. | m g丙烯和戊烯的混合物中共用电子对数为$\frac{3m}{14}$NA |
5.少量铁片与 l00mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加 H2O
②加 KNO3溶液
③滴入几滴浓盐酸
④加入少量铁粉
⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
⑧改用 10mL 0.1mol/L 盐酸.
①加 H2O
②加 KNO3溶液
③滴入几滴浓盐酸
④加入少量铁粉
⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
⑧改用 10mL 0.1mol/L 盐酸.
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ③⑥⑦⑧ |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4 L H2O含有分子数为NA | |
| B. | 分子总数为NA的N2、CO混合气体体积约为22.4 L,质量为28 g | |
| C. | 常温常压下,1.6 g CH4含原子数为0.5NA | |
| D. | 4 g金属钙变成钙离子时失去的电子数目为0.1 NA |
9.25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是 393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
| A. | C(s)+O2(g)═CO(g);△H=-393.5 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=+571.6 kJ/mol | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-890.3 kJ/mol | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2 (g)+3H2O(l);△H=-1400 kJ/mol |