题目内容
1.体积比为1:2:3的氯化钠、氯化镁和氯化铝溶液,分别加入等体积、等浓度的硝酸银溶液,均恰好完全反应生成氯化银沉淀,则这三种溶液的物质的量浓度之比为36:9:4.分析 分别加入等体积、等浓度的硝酸银溶液,均恰好完全反应生成氯化银沉淀,存在NaCl~$\frac{1}{2}$MgCl2~$\frac{1}{3}$AlCl3~AgCl↓,以此来解答.
解答 解:设生成AgCl为1mol,则
由NaCl~$\frac{1}{2}$MgCl2~$\frac{1}{3}$AlCl3~AgCl↓可知,
氯化钠、氯化镁和氯化铝的物质的量分别为1mol、$\frac{1}{2}$mol、$\frac{1}{3}$mol,
结合c=$\frac{n}{V}$可知,
体积之比为1:2:3,三种溶液的物质的量浓度之比为$\frac{1}{1}$:$\frac{\frac{1}{2}}{2}$:$\frac{\frac{1}{3}}{3}$=36:9:4,
故答案为:36:9:4.
点评 本题考查化学反应的计算,为高频考点,把握氯离子守恒为解答的关键,侧重分析与计算能力的考查,注意关系式法的应用,题目难度不大.

练习册系列答案
相关题目
8.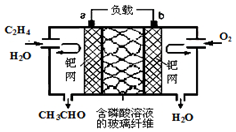 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )| A. | 该装置能量转化形式是电能转化为化学能 | |
| B. | 负极反应式为:CH2=CH2-2e-+H2O=CH3CHO+2H+ | |
| C. | 每有0.1 mol O2反应,则向负极迁移的H+的物质的量为0.4 mol | |
| D. | 电子移动方向:电极a→磷酸溶液→电极b |
12.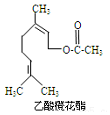 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
| A. | ①②③ | B. | ①②⑤ | C. | ①②⑤⑥ | D. | ①②④⑤ |
13.白磷的化学式写成P,但其实际组成为P4,而三氧化二磷其实是以六氧化四磷的形式存在的,已知P4O6分子中只含有单键,且每个原子的最外层都满足8电子结构,则分子中含有的共价键的数目是( )
| A. | 10 | B. | 12 | C. | 24 | D. | 28 |
10.已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )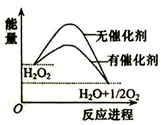

| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+O2 △H<0 | |
| D. | 断键吸收的总能量小于成键放出的总能量 |