��Ŀ����
��10�֣�
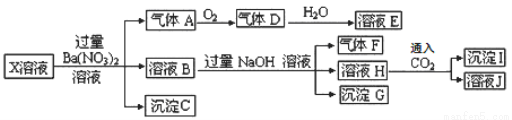
��1���Ʊ�������������Ļ�ѧ����ʽΪ ��
��2��̼��������ˮ��Һ�еĵ��뷽��ʽΪ ��
��3����֤��Na2SO3��Һ�д���SO32��+H2O HSO3��+OH��ˮ��ƽ�����ʵ�� ����ѡ����ĸ����
HSO3��+OH��ˮ��ƽ�����ʵ�� ����ѡ����ĸ����
A�������̪��Һ��죬�ټ���H2SO4��Һ���ɫ��ȥ
B�������̪��Һ��죬�ټ�����ˮ���ɫ��ȥ
C�������̪��Һ��죬�ټ���BaCl2��Һ����������Һ�ɫ��ȥ
��4�����п��淴Ӧ��2A(g)��2B(g) C(g)��3D(s)�����ܱ��������ݻ����¶ȶ���ͬ�������£��ֱ����������;������ƽ�⣺��. A��B����ʼ���ʵ�����Ϊ2 mol����.C��D����ʼ���ʵ����ֱ�Ϊ2 mol��6 mol������˵������ȷ���� ����ѡ����ĸ����
C(g)��3D(s)�����ܱ��������ݻ����¶ȶ���ͬ�������£��ֱ����������;������ƽ�⣺��. A��B����ʼ���ʵ�����Ϊ2 mol����.C��D����ʼ���ʵ����ֱ�Ϊ2 mol��6 mol������˵������ȷ���� ����ѡ����ĸ����
A��������;�����մﵽƽ��ʱ����ϵ�ڻ������İٷ������ͬ
B���ﵽƽ��ʱ��;�������û�����ܶ�Ϊ;�������û�����ܶȵ�2��
C���ﵽƽ��ʱ��;����C��ƽ��Ũ�ȴ���;����C��ƽ��Ũ�ȵ�2��
��5���ں��ݾ��ȣ�������罻�������������½���2A (g)+ B(g) 2C(g)+ D(s)��Ӧ�����±�����Ͷ�ϣ���Ӧ�ﵽƽ��״̬�������ϵѹǿ���ߡ������÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��ϵ�� ��
2C(g)+ D(s)��Ӧ�����±�����Ͷ�ϣ���Ӧ�ﵽƽ��״̬�������ϵѹǿ���ߡ������÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��ϵ�� ��
���� | A | B | C | D |
��ʼͶ��/mol | 2 | 1 | 2 | 0 |
��1�� FeCl3 + 3H2O  Fe(OH)3 (����)+ 3HCl ��2�֣�
Fe(OH)3 (����)+ 3HCl ��2�֣�
��2�� NaHCO3 = Na+ + HCO3 - ��2�֣�
��3��C ��2�֣�
��4�� C ��2�֣�
��5��K���¶ȵ����߶���С��2�֣�
��������
�����������1���Ȼ����ڷ�ˮ��ˮ���Ʊ����壬�Ʊ���ӦΪFeCl3+3H2O Fe��OH��3�����壩+3HCl��
Fe��OH��3�����壩+3HCl��
��2��̼������Ϊǿ����ʣ���ˮ��Һ�еĵ��뷽��ʽΪNaHCO3=Na++HCO3-��
��3��A�������̪��Һ��죬�ټ���H2SO4��Һ��Ӧ���������ơ�ˮ�Ͷ���������ȷ��ˮ��ƽ��Ĵ��ڣ�����B�������̪��Һ��죬�ټ�����ˮ����������ԭ��Ӧ�����������ƣ�����ˮ��HClO����Ư���ԣ�����ȷ��ˮ��ƽ��Ĵ��ڣ�����C�������̪��Һ��죬�ټ���BaCl2��Һ��SO32-+H2O?HSO3-+OH-ˮ��ƽ�������ƶ������������Һ�ɫ��ȥ����ȷ��
��4�����ܱ��������ݻ����¶ȶ���ͬ�������£��ֱ����������;������ƽ�⣺��A��B����ʼ���ʵ�����Ϊ2mol����C��D����ʼ���ʵ����ֱ�Ϊ2mol��6mol������;��II����ת��ΪA��B��A��B����ʼ���ʵ�����Ϊ4mol������Ϊ��Чƽ�⣬��DΪ���壬II��ѹǿ��ƽ�������ƶ�����A��������;�����մﵽ��ƽ��Ϊ��Чƽ�⣬II��ѹǿ��ƽ�������ƶ������ƴ�����ϵ�ڸ��������İٷ���ɲ���ͬ������B���ﵽƽ��ʱ��DΪ���壬���������������С�ڢ��2�����������ݻ���ͬ����;�������û�����ܶ�С��;�������û�����ܶȵ�2��������C���ﵽƽ��ʱ������ƽ��Ϊ��Чƽ�⣬���ڢ��г�ʼ��Ӧ��Ϊ���2����II��ѹǿ������C����I�ж��2�����������ݻ���ͬ���ﵽƽ��ʱ��;����C��ƽ��Ũ�ȴ���;����C��ƽ��Ũ�ȵ�2������ȷ��
��5������ʼD�����ʵ���Ϊ0��֪����Ӧ2A ��g��+B��g��?2C��g��+D��s��������Ӧ���н���ƽ�⣬����Ӧ�����������С�ķ�Ӧ��������������䣬ƽ��ʱѹǿ���ʾ��������£����������¶����ߣ�������ӦΪ���ȷ�Ӧ�������¶�ƽ�����淴Ӧ���У���ѧƽ�ⳣ����С��
���㣺���⿼�黯ѧƽ����жϺ��ƶ�������ʽ����д����Чƽ�⡢��ѧƽ�ⳣ����

 �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
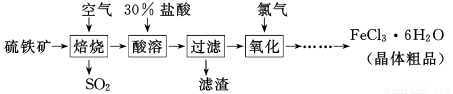
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д���13�֣�ʵ������������������Ʊ��������������й����ʵ�����������±���
������ | ��Է������� | �ܶ�/g��cm-3 | �е㣬/�� | �ܽ��/l00gˮ |
������ | 74 | 0.80 | 118.0 | 9 |
������ | 60 | 1.045 | 118.1 | ���� |
���������� | 116 | 0.882 | 126.1 | 0��7 |
�������£�
����50mL������ƿ�У�����18.5 mL��������13.4 mL�����ᣬ 3��4��Ũ���ᣬͶ���ʯ����װ��ˮ�������ã�ʵ������в��Ϸ����ȥ��Ӧ���ɵ�ˮ�����¶ȼƼ����������ܡ�
�ڽ���ˮ���ֳ�������ͷ�ӦҺһ�����Һ©���У�ˮϴ�� 10% Na2CO3ϴ�ӣ���ˮϴ�����ת������ƿ�����
�۽�����������������������ƿ�У���ѹ�����ռ���֣���15.1 g������������

��ش��й����⣺
��1����ˮӦ�ô������� ����a��b���˹ܿ�ͨ�롣
��2������A�з�����Ӧ�Ļ�ѧ����ʽΪ____ ��
��3������١����Ϸ����ȥ��Ӧ���ɵ�ˮ���ò�����Ŀ���ǣ� ��
��4�����������10%Na2CO3��Һϴ���л��㣬�ò�������Ŀ���� ��
��5�����з�Һ����ʱ��ʹ�õ�©����____ ����ѡ���
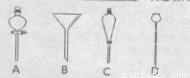
��6��������ڽ����������ʱ������118�濪ʼ�ռ���֣�����ƫ___ ����ߡ����ߡ��͡���ԭ����____
��7����ʵ������У����������������IJ����� ��
����ʵ�顰�����������롰���ۡ���Ӧ��ϵ��ȷ����
| ���������� | ���� |
A | ��װ��Fe(NO3)2��Һ���Թ��м���ϡH2SO4,�ڹܿڹ۲쵽����ɫ���� | HNO3�ֽ�������NO2 |
B | �������Һ�м���ϡH2SO4�����ȼ����ӣ���ȴ���ټ�������Cu(OH)2��Һ�����ȣ�û�к�ɫ�������� | ����û��ˮ��������� |
C | ��Na2CO3��Һ��ͨ������CO2 ����Һ����� | ������NaHCO3 |
D | ����ˮ�Ҵ��м���ŨH2SO4��������170�����������ͨ������KMnO4��Һ����ɫ��ȥ | ʹ��Һ��ɫ����������ϩ |
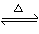 2SO3(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
2SO3(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ��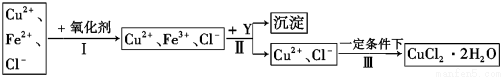
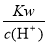 =10-13mol��L-1��Һ�У�Fe3+��NH4����Mg2+�� SO42-
=10-13mol��L-1��Һ�У�Fe3+��NH4����Mg2+�� SO42-