题目内容
18.室温下,0.01mol/L二元酸H2A溶液的pH=3,下列说法正确的是( )| A. | 该溶液中由水电离出的c(H+)为1.0×10-3mol/L | |
| B. | 在Na2A、NaHA两种溶液中,离子种类不同 | |
| C. | 在NaHA溶液中一定有c(OH-)+c(HA-)+2c(A2-)═c(Na+)+c(H+) | |
| D. | 在Na2A溶液中,c(Na+)>c(HA-)>c(A2-)>c(OH-)>c(H+) |
分析 常温下,0.01mol/L二元酸H2A溶液的pH=3,溶液中氢离子浓度小于酸浓度,则该酸是二元弱酸,
A.结合溶液中离子积常数计算Kw=10-14;
B.在Na2A溶液中酸根离子分两步水解,NaHA中HA-离子既水解又电离;
C.任何电解质溶液中都存在电荷守恒;
D.在Na2A溶液中A2-离子分步水解,溶液显碱性.
解答 解:A.0.01mol/L二元酸H2A溶液的pH=3,水电离出氢离子浓度1.0×10-11mol/L,故A错误;
B.在Na2A溶液中A2-分两步水解,第一步水解生成HA-,第二步水解生成H2A,NaHA中HA-离子既水解生成H2A又电离生成A2-,任何溶液中都存在氢离子和氢氧根离子,所以两种溶液中离子种类相同,故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),故C正确;
D..在Na2A溶液中A2-离子分步水解,溶液显碱性,溶液中离子浓度大小c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+),故D错误;
故选C.
点评 本题考查了弱电解质的电离、盐类水解,明确弱电解质的电离、盐类水解特点是解本题关键,先根据酸浓度与pH关系确定酸的强弱,再结合电荷守恒来分析解答,题目难度中等.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
9.某装置如图所示,则下列说法中正确的是( )


| A. | 该装置能够将化学能转化为电能 | B. | 左侧烧杯中没有化学反应发生 | ||
| C. | 该装置中的灯泡会发光 | D. | 左侧烧杯中有气体生成 |
3.下列实验操作正确的是( )
| A. | 蒸发操作时,应将溶液完全蒸干后停止加热 | |
| B. | 稀释浓硫酸时,沿烧杯内壁将浓硫酸缓慢加入水中,边加边搅拌 | |
| C. | 分液操作时,先放出下层液体,再关闭活塞,从漏斗口倒出上层液体 | |
| D. | 配制一定物质的量浓度的溶液时,若加水超过容量瓶的刻度线,用胶头滴管吸出多余液体 |
10.下列说法不正确的是( )
| A. | 乙烯、乙炔、乙醛都能使溴水或酸性KMnO4溶液褪色 | |
| B. | 可用加入NaOH溶液并加热,通过观察油层是否消失或变薄来鉴别苯和乙酸乙酯 | |
| C. | 可用H2SO4溶液、银氨溶液和碘水来检验淀粉液是否部分水解 | |
| D. | 油脂在热NaOH溶液中完全水解后,加入饱和食盐水,可观察到液面上有固体析出 |
7.下列存放物质的方法中错误的是( )
| A. | Na可保存在CCl4中 | |
| B. | NaOH溶液盛装在带橡皮塞的试剂瓶中 | |
| C. | 用棕色细口试剂瓶存放氯水 | |
| D. | 漂白粉要密闭在容器中保存 |
3.101kPa时,S(s)+O2(g)═SO2(g)△H=-297.23kJ•mol-1.据此分析,下列说法中不正确的是( )
| A. | S的燃烧热为297.23 kJ•mol-1 | |
| B. | S升华是吸热过程 | |
| C. | 形成1 mol SO2的化学键释放的总能量大于断裂1 mol S(s)和1 mol O2(g)的化学键所吸收的总能量 | |
| D. | S(g)+O2(g)═SO2(g)放出的热量小于297.23 kJ |
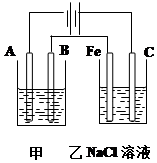 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: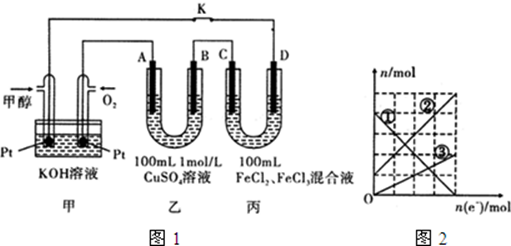
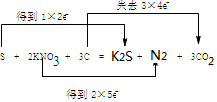 (同时用双线桥表示电子的得失)
(同时用双线桥表示电子的得失)