题目内容
在一定的温度和压强下,合成氨反应3H2+N2?2NH3达到平衡时,若恒温恒压条件下分别充入NH3和N2对平衡会产生什么影响?请说明理由.
考点:化学平衡的影响因素
专题:化学平衡专题
分析:平衡状态时,恒温恒压条件下分别充入NH3和N2时,导致其浓度增大,依据浓度对化学平衡的影响分析.
解答:
解:在一定的温度和压强下,合成氨反应3H2+N2?2NH3达到平衡时,若恒温恒压条件下充入NH3,因为氨气浓度增大,据勒夏特列原理,平衡向氨气浓度减小的方向移动,即向逆反应方向移动;若恒温恒压条件下充入N2,因为氮气浓度增大,据勒夏特列原理,平衡向氮气浓度减小的方向移动,即向正反应方向移动,
答:充入NH3,平衡向逆反应方向移动,因为充入氨气时氨气浓度增大,据勒夏特列原理,平衡向氨气浓度减小的方向移动,即向逆反应方向移动;
充入N2,平衡向正反应方向移动,因为充入氮气时氮气浓度增大,据勒夏特列原理,平衡向氮气浓度减小的方向移动,即向正反应方向移动.
答:充入NH3,平衡向逆反应方向移动,因为充入氨气时氨气浓度增大,据勒夏特列原理,平衡向氨气浓度减小的方向移动,即向逆反应方向移动;
充入N2,平衡向正反应方向移动,因为充入氮气时氮气浓度增大,据勒夏特列原理,平衡向氮气浓度减小的方向移动,即向正反应方向移动.
点评:本题考查了勒夏特列原理的应用,浓度对化学平衡的影响,题目难度中等.

练习册系列答案
相关题目
在0.5mol Ba(NO3)2中含有NO3-的数目是( )个.
| A、3.01×1023 |
| B、6.02×1023 |
| C、0.5 |
| D、1 |
下列化学用语书写正确的是( )
| A、次氯酸的电离方程式:HClO?H++ClO- |
| B、铝溶于烧碱溶液的离子方程式:Al+2OH-=AlO2-+H2↑ |
| C、电解精炼铜的阴极反应式:Cu-2e-=Cu2+ |
| D、已知中和热为57.3 kJ?mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH (aq)═Na2SO4 (aq)+2H2O ( l )△H=-57.3 kJ?mol-1 |
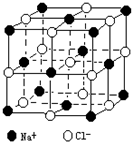 随着科学技术的发展,阿佛加德罗常数的测定手段越来越多,测定的精度也越来越高.现有一种简单可行的测定方法,具体步骤为:
随着科学技术的发展,阿佛加德罗常数的测定手段越来越多,测定的精度也越来越高.现有一种简单可行的测定方法,具体步骤为: