题目内容
|
已知2H2(g)+O2(g) | |
| [ ] | |
A. |
1∶3 |
B. |
3∶1 |
C. |
1∶4 |
D. |
1∶1 |
答案:B
解析:
解析:
|
思路与技巧:可根据所给热化学方程式及反应热数值分别求出1 mol H2和1 mol C3H8完全燃烧各自放出的热量,然后再求混合物的组成. 解法1:设H2的物质的量为x,则C3H8的物质的量为5-x,则285.8×x+(5-x)×2220=3847 kJ.所以x=3.75 mol,由体积之比等于物质的量之比:3.75∶(5-3.75)=3∶1选B. 解法2:据题意1 mol H2燃烧放热571.6/2=285.8 kJ,1 mol C3H8燃烧放热为2220.0 kJ,1 mol混合气体燃烧放热为3847/5=769.4 kJ,由十字交叉法: 解法3:淘汰法求解.分析:当混合气中氢气与丙烷体积比为1∶1,即丙烷为2.5 mol时,热量就已超过3847 kJ,所以当体积比为1∶3,1∶4即丙烷的物质的量大于2.5 mol时将更超过3847 kJ,所以只有3∶1正确. 评析:三种方法中法3最巧,是一种极限思想解题的方法,但不容易想到,而法1和法2实际是一种方法,只是法2中的十字交叉法是法1的一种简略的数学处理,最常用的方法是法2.利用“十字交叉法”求解时,必须将各热量数值换算成1 mol某物质产生的,且最终结果为物质的量之比.对于气体来说,等于体积比. |

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
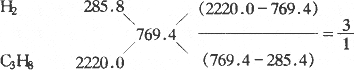




 则△H1>△H2
则△H1>△H2