题目内容
A、B、C、D是由下面的一种阳离子和一种阴离子组成的化合物(阳离子: 、Na+、H+,阴离子:Cl-、OH-、
、Na+、H+,阴离子:Cl-、OH-、 ),在水溶液中它们均抑制水电离.常温下各物质从1mL稀释到1000mL,PH的变化如图1所示,请回答:
),在水溶液中它们均抑制水电离.常温下各物质从1mL稀释到1000mL,PH的变化如图1所示,请回答:
(1)根据图1的PH变化关系写出化学式:A______,C______.
(2)B与过量的D反应生成E,写出该反应的离子方程式______.
(3)E的溶液显______(填“中性”、“酸性”或“碱性”),其原因是______.
(4)图2是室温时向25mL某浓度的C溶液中逐渐滴加O.25mol/L,A溶液过程中PH的变化曲线.G点呈中性,此时,V(A)的体积______10Ml(填“=”、“>”或“<”).H点离子浓度由大到小的顺序是______.
(5)已知BaC2O4的溶度积常数KSP=1.6×10-7.向0.01mol/L的Na2C2O4溶液中加入等体积一定浓度的BaCl2溶液,若要产生沉淀,BaCl2溶液浓度至少为______.
【答案】分析:(1)根据阳离子和阴离子结合形成的物质是强还是弱电解质以及稀释后其酸碱性的变化知识来回答;
(2)根据草酸和氢氧化钠之间发生的是中和反应来回答;
(3)HC2O4-的电离程度大于水解程度,所以草酸氢钠显酸性;
(4)根据氨水和草酸之间反应的量的关系来回答;
(5)根据沉淀溶度积常数来计算.
解答:解:(1)根据强酸稀释为原来的1000倍,则PH在原来的基础上加3,强碱稀释为原来的1000倍,则PH在原来的基础上减3,弱酸稀释为原来的000倍,则PH比原来的基础上加3要小,弱碱稀释为原来的1000倍,则PH比原来的基础上减3要大,根据图中数据可以得出:A是NH3?H2O,B是NaOH,C是HCl,D是H2C2O4,E是Na2C2O4,故答案为:NH3?H2O;HCl;
(2)草酸和氢氧化钠之间发生的是中和反应,当酸过量时生成的是酸式盐,即H2C2O4+OH-=HC2O4-+H2O,
故答案为:H2C2O4+OH-=HC2O4-+H2O;
(3)在草酸氢钠中,由于HC2O4-的电离程度大于水解程度,所以溶液显酸性,
故答案为:酸;HC2O4-的电离程度大于水解程度;
(4)向25mL某浓度的盐酸溶液中逐渐滴加O.25mol/L氨水溶液,当溶液显中性是,则氨水稍过量,所以氨水的体积大于10mL,当加入25mL的氨水时,则水溶液显碱性,是氯化铵和氨水的混合物,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+)(氯化铵的量多于氨水时),c(NH4+)>c(OH-)>c(Cl-)>c(H+)(氯化铵的量少于氨水时),
故答案为:>;c(NH4+)>c(Cl-)>c(OH-)>c(H+)或c(NH4+)>c(OH-)>c(Cl-)>c(H+).
(5)根据草酸钡的Ksp=[Ba2+][C2O42-],0.01mol/L的Na2C2O4溶液中加入等体积一定浓度的BaCl2溶液,若要产生沉淀,Ba2+的浓度为 =
= =3.2×10-5mol/L,故答案为:3.2×10-5mol/L.
=3.2×10-5mol/L,故答案为:3.2×10-5mol/L.
点评:本题重点考查了盐的水解知识的应用,可以根据所学知识进行回答,难度较大,综合性较强.
(2)根据草酸和氢氧化钠之间发生的是中和反应来回答;
(3)HC2O4-的电离程度大于水解程度,所以草酸氢钠显酸性;
(4)根据氨水和草酸之间反应的量的关系来回答;
(5)根据沉淀溶度积常数来计算.
解答:解:(1)根据强酸稀释为原来的1000倍,则PH在原来的基础上加3,强碱稀释为原来的1000倍,则PH在原来的基础上减3,弱酸稀释为原来的000倍,则PH比原来的基础上加3要小,弱碱稀释为原来的1000倍,则PH比原来的基础上减3要大,根据图中数据可以得出:A是NH3?H2O,B是NaOH,C是HCl,D是H2C2O4,E是Na2C2O4,故答案为:NH3?H2O;HCl;
(2)草酸和氢氧化钠之间发生的是中和反应,当酸过量时生成的是酸式盐,即H2C2O4+OH-=HC2O4-+H2O,
故答案为:H2C2O4+OH-=HC2O4-+H2O;
(3)在草酸氢钠中,由于HC2O4-的电离程度大于水解程度,所以溶液显酸性,
故答案为:酸;HC2O4-的电离程度大于水解程度;
(4)向25mL某浓度的盐酸溶液中逐渐滴加O.25mol/L氨水溶液,当溶液显中性是,则氨水稍过量,所以氨水的体积大于10mL,当加入25mL的氨水时,则水溶液显碱性,是氯化铵和氨水的混合物,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+)(氯化铵的量多于氨水时),c(NH4+)>c(OH-)>c(Cl-)>c(H+)(氯化铵的量少于氨水时),
故答案为:>;c(NH4+)>c(Cl-)>c(OH-)>c(H+)或c(NH4+)>c(OH-)>c(Cl-)>c(H+).
(5)根据草酸钡的Ksp=[Ba2+][C2O42-],0.01mol/L的Na2C2O4溶液中加入等体积一定浓度的BaCl2溶液,若要产生沉淀,Ba2+的浓度为
 =
= =3.2×10-5mol/L,故答案为:3.2×10-5mol/L.
=3.2×10-5mol/L,故答案为:3.2×10-5mol/L.点评:本题重点考查了盐的水解知识的应用,可以根据所学知识进行回答,难度较大,综合性较强.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目

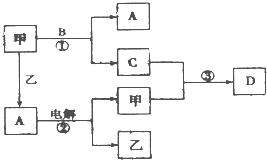 A、B、C、D是由短周期元素组成的四种常见的化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图所示的转化关系:
A、B、C、D是由短周期元素组成的四种常见的化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图所示的转化关系: (2010?柳州三模)A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图反应关系:
(2010?柳州三模)A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图反应关系: