题目内容
2. TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )| A. | 该装置可以将光能转化为电能,同时也能转化为化学能 | |
| B. | 铂电极上发生的反应为:H2-2e-=2H+ | |
| C. | 该装置工作时,电流由TiO2电极经R流向铂电极 | |
| D. | 该装置工作时,TiO2电极附近溶液的pH变大 |
分析 该装置中是将光能转化为电能,然后通过电解将电能转化为化学能,根据图片知,铂电极为阴极,电极反应式为2H++2e-═H2↑,二氧化钛电极为阳极,电极反应式为4OH--4e-=O2↑+2H2O,据此分析解答.
解答 解:A、在光照下TiO2分解水,同时提供电能,所以该装置可以将光能转化为电能,同时电能转化为化学能,故A正确;
B.铂电极为阴极,电极反应式为2H++2e-═H2↑,故B错误;
C.该装置工作时,Pt作阴极、二氧化钛作阳极,阳极上失电子、阴极上得电子,所以电流由铂电极经R流向TiO2电极,故C错误;
D.二氧化钛电极为阳极,电极反应式为4OH--4e-=O2↑+2H2O,TiO2电极附近溶液的pH变小,故D错误;
故选A.
点评 本题考查原电池原理,明确书写各个电极反应式是解本题关键,易错选项是C,根据得失电子确定电流方向,为易错点.

练习册系列答案
相关题目
3.下列叙述正确的是( )
| A. | 苯与溴水充分振荡后,溴水层褪色说明苯分子中的碳原子没有饱和 | |
| B. |  的最简式相同 的最简式相同 | |
| C. | 苯分子是环状结构,只有6个碳原子在同一平面上 | |
| D. | 苯的邻位二元取代物只有一种可以说明苯分予不具有碳碳单键和碳碳双键的交替结构 |
13.已知反应:①2C(s)+O2(g)=2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热为△H=-110.5 kJ/mol | |
| B. | 1molC(s)所具有的能量一定高于1molCO(g)所具有的能量 | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为△H=-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,也放出57.3 kJ 热量 |
10.已知X、Y、Z三种醇互为同系物,则建立在假设基础上的推断正确的是( )
| 假设 | 推断 | |
| A | 若X、Y均能发生消去反应 | Z一定能发生消去反应 |
| B | 若X是白酒的主要成分 | Y可能是丙三醇 |
| C | 若X、Y分子中分别有1个、2个碳原子 | Z的摩尔质量不小于60 g•mol-1 |
| D | 若X、Y均存在醇类同分异构体 | Z一定存在醇类同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
17.下列原子或原子团不属于官能团的是( )
| A. | -CH3 | B. | -F | C. | -OH | D. | 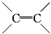 |
7.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷制环己烯;由丙烯制1,2-二溴丙烷 | |
| D. | 由乙烯制聚乙烯;由1,3-丁二烯合成顺丁橡胶 |
14.电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:答下列有关问题:
(1)预测周期表中电负性最大的元素应为F;估计钙元素的电负性的取值范围:0.8<X<1.2
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是同主族自上而下电负性降低.
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键,其理由是因为AlCl3中Cl与Al的电负性差值为1.5,小于1.7,则AlCl3的键为共价键.而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值也小于1.7,即AlBr3的键为共价键.
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是同主族自上而下电负性降低.
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键,其理由是因为AlCl3中Cl与Al的电负性差值为1.5,小于1.7,则AlCl3的键为共价键.而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值也小于1.7,即AlBr3的键为共价键.
12.下列实验能获得成功的是( )
| A. | 苯和浓溴水混合加入铁作催化剂制溴苯 | |
| B. | 将苯和浓硝酸混合共热制硝基苯 | |
| C. | 可用分液漏斗分离硝基苯和水 | |
| D. | 乙烯通入溴的四氯化碳溶液中获得1,1-二溴乙烷 |