题目内容
15.下列各项中表达正确的是考( )| A. | 基态氧原子核外价电子的轨道表示式: | |
| B. | HClO的结构式为H-Cl-O | |
| C. | 用电子式表示NaCl的形成过程: | |
| D. | F-的结构示意图: |
分析 A.基态氧原子的2p轨道上电子错误;
B.HClO中O原子形成2个共价键;
C.NaCl是离子化合物,在形成过程中存在电子得失;
D.F-的核内有9个质子,核外有10个电子.
解答 解:A.基态氧原子核外价电子的轨道表示式: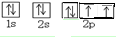 ,故A错误;
,故A错误;
B.HClO中O原子形成2个共价键,则HClO的结构式为H-O-Cl,故B错误;
C.氯化钠为离子化合物,钠离子与氯离子通过离子键结合而成,NaCl的形成过程为 ,故C错误;
,故C错误;
D.F-的核内有9个质子,核外有10个电子,则F-的结构示意图: ,故D正确.
,故D正确.
故选D.
点评 本题考查了轨道式、电子式、结构式等化学用语的判断,题目难度中等,注意掌握常见化学用语的表示方法,明确结构简式、离子化合物与共价化合物的电子式的区别,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
6.下列描述中正确的是( )
| A. | CO2为V形的极性分子 | |
| B. | SO2与O3互为等电子体 | |
| C. | NaCl的晶格能高于KCl | |
| D. | 第一电离能由高到低的顺序为:F>O>N |
20.下列叙述正确的是( )
| A. | 由同种元素组成的物质肯定是纯净物 | |
| B. | 一种元素可形成多种离子 | |
| C. | 含有金属元素的离子一定都是阳离子 | |
| D. | 具有相同质子数的粒子都属于同种元素 |
4.将pH为5的盐酸溶液稀释500倍,稀释后溶液中c(Cl-)和c(H+)之比约为( )
| A. | 1:2 | B. | 1:5 | C. | 1:10 | D. | 10:1 |
5.胶体分散系在日常生活中很常见.下列说法不正确的是( )
| A. | 将饱和的FeCl3溶液滴入沸水中形成Fe(OH)3胶体 | |
| B. | 蛋白质溶液可观察到丁达尔现象 | |
| C. | Fe(OH)3胶体可观察到丁达尔现象 | |
| D. | 胶体分散系中所有粒子的直径都不在1~100 nm之间 |

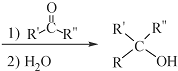
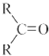 $\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$
$\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$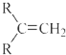 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢)  .写出A中含氧官能团的名称:羟基
.写出A中含氧官能团的名称:羟基 或
或 .(不考虑环状结构)
.(不考虑环状结构) .
.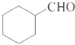 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH.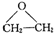 ,该反应的原子利用率为100%,反应的化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$
,该反应的原子利用率为100%,反应的化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$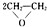 .
.