题目内容
14.徐光宪在《分子共和国》一书中介绍了许多明星分子,如H2O2、CO2、BF3、CH3COOH等.下列说法正确的是( )| A. | H2O2分子的空间构型为直线形 | |
| B. | CO2分子为非极性分子 | |
| C. | BF3分子中的B原子满足8电子稳定结构 | |
| D. | CH3COOH分子中C原子均为sp3杂化 |
分析 A.H2O2分子中O原子形成2个σ键、含有2对孤对电子,氧原子与连接的原子形成V形结构;
B.CO2分子为直线型对称结构,分子中正负电荷重心重合;
C.共价键化合物中原子最外层电子数+|化合物中该元素化合价|=8,该原子满足8电子稳定结构;
D.羧基中C原子形成3个σ键、没有孤对电子,杂化轨道数目为3.
解答 解:A.H2O2分子中O原子形成2个σ键、含有2对孤对电子,氧原子与连接的原子形成V形结构,H2O2分子的空间构型不可能为直线形,实际为展开书页型结构,故A错误;
B.CO2分子为直线型对称结构,分子中正负电荷重心重合,属于非极性分子,故B正确;
C.BF3分子中的F原子满足8电子结构,B原子不满足8电子稳定结构,故C错误;
D.甲基中碳原子形成4个σ键,没有孤对电子,采取sp3杂化,羧基中C原子形成3个σ键、没有孤对电子,杂化轨道数目为3,为sp2杂化,故D错误,
故选:B.
点评 本题考查杂化方式与空间构型判断、分子极性、共价键等,理解掌握应用价层电子对互斥理论与杂化轨道理论判断微粒空间构型.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
4.下列实验的操作、现象、解释或结论都正确的是( )
| 选项 | 操作、现象 | 解释或结论 |
| A | 某溶液中先加稀HCl酸化,再加AgNO3,产生白色沉淀 | 原溶液有Cl-存在 |
| B | Cl2能使湿润的红布条褪色 | Cl2具有漂白性 |
| C | Na2SiO3溶液中通入CO2产生白色胶状沉淀 | H2CO3酸性大于H2SiO3 |
| D | 光照氯水有气泡产生 | 该气体一定是Cl2 |
| A. | A | B. | B | C. | C | D. | D |
5.已知:Pb元素在化合物中有+4和+2两种价态:Pb02受热分解可生成Pb304、Pb0和O2:+4价的Pb能氧化浓盐酸生成Cl2 PbO能与浓盐酸反应但不能将其氧化.现将1.4mol Pb02加热一段时间分解得到O2和固体甲,向甲中加入足量的浓盐酸得到Cl2.反应生成的O2和Cl2的物质的盘之比为2:3,下列说法正确的是 ( )
| A. | 甲可能是Pb304和PbO的混合物 | |
| B. | 整个反应过程中转移电子的总量为2.1mol | |
| C. | 若甲与浓盐酸充分反应,则需要消耗HCl的总量为2.8 mol | |
| D. | 甲中各物质的物质的量之比可能是n(PbO2):n(Pb304):n(PbO)=3:3:2 |
2.下列有关说法正确的是( )
| A. | 明矾和硫酸铁均可用作净水剂 | |
| B. | 有单质参加的化学反应一定是氧化还原反应 | |
| C. | 溶液因不带电而稳定,胶体因带电而不稳定 | |
| D. | 相同质量的铝粉,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比是1:3 |
9.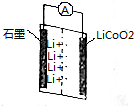 某锂离子二次电池装置如图所示,其放电时的总反应为Li1-xCoO2+LixC6═6C+LiCoO2.下列说法正确的是( )
某锂离子二次电池装置如图所示,其放电时的总反应为Li1-xCoO2+LixC6═6C+LiCoO2.下列说法正确的是( )
 某锂离子二次电池装置如图所示,其放电时的总反应为Li1-xCoO2+LixC6═6C+LiCoO2.下列说法正确的是( )
某锂离子二次电池装置如图所示,其放电时的总反应为Li1-xCoO2+LixC6═6C+LiCoO2.下列说法正确的是( )| A. | 石墨为正极 | |
| B. | 充电时,阳极质量不变 | |
| C. | 充电时,阴极反应式为xLi-xe-═xLi+ | |
| D. | 放电时,正极反应为xLi+Li1-xCoO2+xe-═LiCoO2 |
19.以甲基橙为指示剂,用盐酸滴定NaOH溶液至终点时颜色变化为( )
| A. | 橙色变为黄色 | B. | 黄色变为橙色 | C. | 橙色变为红色 | D. | 红色变为橙色 |
3.对二甲苯 ( PX )是生产矿泉水瓶 (聚对苯二甲酸乙二酯,简称 PET )的必要原料,生产涉及的反应之一如下:5 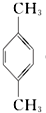 (PX)+12MnO${\;}_{4}^{-}$+36H+→5
(PX)+12MnO${\;}_{4}^{-}$+36H+→5 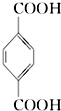 (PTA)+12Mn2++28H2O,下列有关说法错误的是( )
(PTA)+12Mn2++28H2O,下列有关说法错误的是( )
 (PX)+12MnO${\;}_{4}^{-}$+36H+→5
(PX)+12MnO${\;}_{4}^{-}$+36H+→5  (PTA)+12Mn2++28H2O,下列有关说法错误的是( )
(PTA)+12Mn2++28H2O,下列有关说法错误的是( )| A. | PTA 是该反应的氧化产物 | |
| B. | PTA 与乙二醇通过加聚反应即可生产 PET 塑料 | |
| C. | PX 分子含有苯环的同分异构体还有 3 种 | |
| D. | 该反应消耗 1molPX,共转移 12N A 个电子 ( NA 为阿伏加德罗常数) |
4.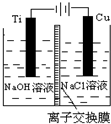 纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制阳极电解液中OH-的浓度制备纳米级Cu2O的装置如图所示,总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法不正确的是( )
纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制阳极电解液中OH-的浓度制备纳米级Cu2O的装置如图所示,总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法不正确的是( )
 纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制阳极电解液中OH-的浓度制备纳米级Cu2O的装置如图所示,总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法不正确的是( )
纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制阳极电解液中OH-的浓度制备纳米级Cu2O的装置如图所示,总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法不正确的是( )| A. | 钛(Ti)电极表面发生氧化反应 | |
| B. | 阳极附近溶液的pH逐渐减小 | |
| C. | 离子交换膜宜采用阴离子交换膜 | |
| D. | 阳极表面总反应式是:2Cu+2OH--2e-═Cu2O+H2O |
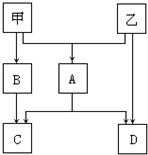 甲、乙是两种常见短周期元素的单质,其有关化合物的性质如图所示,其中C为白色沉淀,D为气体.
甲、乙是两种常见短周期元素的单质,其有关化合物的性质如图所示,其中C为白色沉淀,D为气体.