题目内容
8.实验室欲用NaOH固体配制1.00mol/L的NaOH溶液480mL:(1)配制时,必须使用的玻璃仪器有500mL的容量瓶、烧杯、玻璃棒、胶头滴管.
(2)使用容量瓶前必须进行的一步操作是检查是否漏水.
(3)计算,称量.要完成本实验该同学应称出NaOH20.0g.
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是搅拌,加速NaOH溶解.
(5)转移、洗涤.转移时应使用玻璃棒引流,需要洗涤烧杯2~3次是为了将溶质全部转移至容量瓶.
(6)定容,摇匀.
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度.
(8)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是④⑤.
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
分析 (1)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)容量瓶在使用前要先查漏;
(3)由于无480mL容量瓶,所以选择500mL容量瓶,配制出500mL溶液,根据m=cVM来计算;
(4)溶解NaOH时需要使用玻璃棒搅拌,加速NaOH的溶解过程;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶;
(8)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=$\frac{n}{v}$分析判断.
解答 解:(1)没有480mL容量瓶,所以选择500mL容量瓶,操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,用玻璃棒搅拌,加速溶解,恢复室温后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以需要的玻璃仪器有:500mL的容量瓶;烧杯;玻璃棒;胶头滴管;
故答案为:500mL的容量瓶;烧杯;玻璃棒;胶头滴管;
(3)容量瓶有活塞,故在使用前要先检查是否漏水;
故答案为:检查是否漏水;
(3)由于无480mL容量瓶,所以选择500mL容量瓶,配制出500mL溶液,故所需NaOHm=cVM=1.0mol/L×0.5L×40g/mol=20.0g;
故答案为:20.0;
(4)溶解的实验中需要使用玻璃棒进行搅拌,加速NaOH溶解;
故答案为:搅拌,加速NaOH溶解;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶;
故答案为:玻璃棒;将溶质全部转移至容量瓶;
(8)①没有洗涤烧杯和玻璃棒,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠质量减小,所配溶液浓度偏低;
②转移溶液时不慎有少量洒到容量瓶外面,移入容量瓶中的氢氧化钠的质量减小,所配溶液浓度偏低;
③最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
④定容时俯视刻度线,导致溶液体积偏小,所配溶液浓度偏高;
⑤未冷却到室温就将溶液转移到容量瓶并定容,温度恢复室温后,会导致溶液体积偏小,溶液浓度偏高;
⑥摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低.
故选:④⑤.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和操作步骤是解题关键,注意容量瓶的构造及使用方法,题目难度不大.

| A. | 碳棒上放出氯气 | B. | 铁钉上放出氢气 | C. | 碳棒上放出氧气 | D. | 铁钉锈蚀 |
①淀粉是人体所需能量的主要来源,可以用碘水检验淀粉
②油脂可以在酸性条件下水解生成甘油和肥皂
③部分蛋白质遇到浓硝酸会变黄
④甘蔗中含有蔗糖,它和麦芽糖互为同分异构体
⑤糖类、油脂和蛋白质都能发生水解.
| A. | ②③④ | B. | ①③⑤ | C. | ①③④ | D. | ②④⑤ |
| A. |  | B. |  | ||
| C. |  | D. |  |
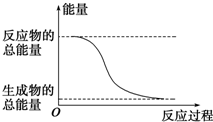
| A. | 用CO在高温条件下还原CuO的反应 | |
| B. | N2(g)+O2(g)═2NO(g)△H=+182.6 kJ•mol-1 | |
| C. | 形成化学键过程中放出862kJ热量的化学反应 | |
| D. | 能量变化如图所示的化学反应 |
| A. | FeS2既是氧化剂又是还原剂 | |
| B. | 被氧化的硫和被还原的硫的质量比为3:7 | |
| C. | 氧化剂只有CuSO4 | |
| D. | 1 mol CuSO4可氧化$\frac{5}{7}$mol的硫 |
| A. | 过氧化氢中既含有极性键又含有非极性键 | |
| B. | 18O原子中含有18个中子 | |
| C. | 含有相同电子数的H2O和NH3的分子数相同 | |
| D. | 苯分子中所有原子共处在同一平面上 |