题目内容
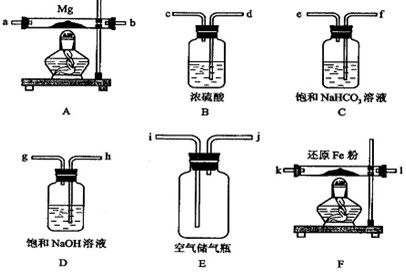
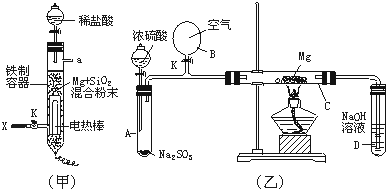
氮化镁(Mg3N2)是一种重要的化合物,它与水作用可以产生NH3。请回答下列问题:(1)Mg3N2的电子式是________________,该化合物是由_______(填“共价”、“离子”或“金属”)键形成的。
(2)Mg3N2与盐酸反应生成____种盐,其电子式分别是_________________________。
(3)比较Mg3N2中两种微粒的半径:r(Mg2+)_________r(N3-)(填“>”、“<”或“=”)。
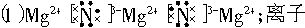
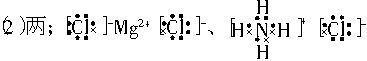
(3)<
【试题分析】
(1)活泼金属和活泼非金属形成的化学键是离子键。Mg是活泼的金属元素(电负性是1.2),且N原子吸引电子的能力较强(电负性3.0),因此Mg和N形成的化学键是离子键。写离子化合物电子式时,阴离子和复杂阳离子要用“[]”括起来,阴、阳离子要间隔写: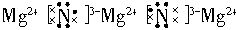 。
。
(2)根据题中信息“氮化镁与水反应可以产生NH3”可知,它与水反应的另一种产物是Mg(OH)2,从而进一步推出它与盐酸反应的产物是MgCl2和NH4Cl。电子式分别为: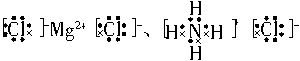
(3)Mg2+与N3-具有相同的电子层结构,核电荷数多的离子半径小。所以,r(Mg2+)<r(N3-)。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目