题目内容
2.1g平均相对分子质量为7.2的CO和H2组成的混和气体在足量的氧气中充分燃烧后,立即通入足量的Na2O2粉未中,待反应完全后,粉未质量可增加( )
| A、2.1g | B、4.2g |
| C、3.6g | D、不能确定 |
考点:有关混合物反应的计算
专题:计算题
分析:利用差量法,根据化学方程式分析:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应;
2CO+O2
2CO2,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2
2H2O,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.
2CO+O2
| ||
2H2+O2
| ||
解答:
解:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应.2CO+O2
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量;
所以2.1gCO和H2的混合气体在足量氧气中充分燃烧后,将产物立即通入盛有足量Na2O2的反应管,
固体质量增重为2.1gCO和H2的混合气体的质量,
故选A.
| ||
2H2+O2
| ||
所以2.1gCO和H2的混合气体在足量氧气中充分燃烧后,将产物立即通入盛有足量Na2O2的反应管,
固体质量增重为2.1gCO和H2的混合气体的质量,
故选A.
点评:本题考查化学方程式的计算,题目难度中等,注意从CO2、H2O与Na2O2生成固体质量的变化分析规律是解答该题的关键.

练习册系列答案
相关题目
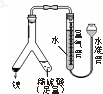 用如图所示实验装置测定某温度下气体摩尔体积,有关叙述错误的是( )
用如图所示实验装置测定某温度下气体摩尔体积,有关叙述错误的是( )| A、将水准管上提,液面高于量气管且不下降,说明装置不漏气 |
| B、可用来测定镁的相对原子质量 |
| C、读取气体体积时水准管的水面高于量气管的水面,可导致测定结果偏高 |
| D、金属镁中含有少量杂质铝,可导致测定结果偏高 |
下列关于水体污染及防治的说法正确的是( )
| A、N和P是植物营养素,海洋或湖泊中N、P含量越高越有利于水生动植物的生长 |
| B、只要不喝被重金属污染的水就不会中毒,因此水中的重金属污染对人类影响不大 |
| C、用熟石灰处理钢铁厂的酸性废水,利用的是复分解反应原理 |
| D、用Na2S处理含Hg2+废水使Hg2+变成HgS沉淀而除去,利用的是氧化还原反应原理 |
将1.0体积乙烷和乙烯的混合气体在氧气中充分燃烧,生成2.0体积的CO2和2.4体积的水蒸气(同温同压下测定).则混合物中烷烃和烯烃的体积比为( )
| A、3:1 | B、1:3 |
| C、2:3 | D、3:2 |
(双项)化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A、为提高农作物的产量和质量,应大量使用化肥和农药 |
| B、绿色化学的核心是从源头上控制污染 |
| C、实现化石燃料清洁利用,就无需开发新能源 |
| D、垃圾是放错地方的资源,应分类回收利用 |
下列做法中,不利于实现让定州“天更蓝,水更清”目标的是( )
| A、推广使用无磷洗涤剂 |
| B、推广使用脱硫煤 |
| C、减少汽车尾气排放 |
| D、任意排放污水 |