题目内容
将下列性质的番号,填入各小题后面对应的括号中:
A.脱水性; B.强酸性; C.吸水性; D.氧化性.
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色.
(2)NaOH与H2SO4反应,可生成Na2SO4和H2O.
(3)在烧杯中放入蔗糖,滴入浓H2SO4变黑.
(4)在冷浓HNO3中放入铝片没明显现象.
(5)浓H2SO4敞口久置会增重.
(6)用稀硫酸清洗金属表面的氧化物. .
A.脱水性; B.强酸性; C.吸水性; D.氧化性.
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色.
(2)NaOH与H2SO4反应,可生成Na2SO4和H2O.
(3)在烧杯中放入蔗糖,滴入浓H2SO4变黑.
(4)在冷浓HNO3中放入铝片没明显现象.
(5)浓H2SO4敞口久置会增重.
(6)用稀硫酸清洗金属表面的氧化物.
考点:浓硫酸的性质
专题:氧族元素
分析:浓硫酸具有吸水性和脱水性,吸水是吸收了混合物中存在的水,而脱水是夺取了物质分子结构中的氧原子和氢原子,且氢氧原子的比例为二比一;
浓硫酸中硫元素处于最高价态,容易得到电子,具有强的氧化性;
硫酸在水中完全电离生成氢离子与硫酸根离子,具有强酸性.
浓硫酸中硫元素处于最高价态,容易得到电子,具有强的氧化性;
硫酸在水中完全电离生成氢离子与硫酸根离子,具有强酸性.
解答:
解:(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色,浓硫酸吸收胆矾中的结晶水,体现吸水性;
(2)NaOH与H2SO4反应,可生成Na2SO4和H2O,反应的实质是氢离子与氢氧根离子反应反应生成水,体现硫酸的酸性;
(3)在烧杯中放入蔗糖,滴入浓H2SO4变黑,浓硫酸夺取蔗糖分子结构中的氧原子和氢原子生成水,体现脱水性;
(4)浓硝酸具有强氧化性,使铁和铝发生钝化,体现浓硝酸的强氧化性;
(5)浓硫酸具有吸水性,敞口久置会增重,体现浓硫酸的吸水性;
(6)稀硫酸与金属氧化物反应生成易溶性的盐和水,体现酸性;
故答案为:(1)C(2)B(3)A(4)D(5)C(6)B.
(2)NaOH与H2SO4反应,可生成Na2SO4和H2O,反应的实质是氢离子与氢氧根离子反应反应生成水,体现硫酸的酸性;
(3)在烧杯中放入蔗糖,滴入浓H2SO4变黑,浓硫酸夺取蔗糖分子结构中的氧原子和氢原子生成水,体现脱水性;
(4)浓硝酸具有强氧化性,使铁和铝发生钝化,体现浓硝酸的强氧化性;
(5)浓硫酸具有吸水性,敞口久置会增重,体现浓硫酸的吸水性;
(6)稀硫酸与金属氧化物反应生成易溶性的盐和水,体现酸性;
故答案为:(1)C(2)B(3)A(4)D(5)C(6)B.
点评:本题考查了硫酸的性质,熟悉硫酸性质是解题关键,注意相关知识的积累.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
现有bXn-和aYm+两种离子,它们的电子层结构相同,则a与下列式子有相等关系的是( )
| A、b-m-n |
| B、b+m+n |
| C、b-m+n |
| D、b+m-n |
下列说法正确的是( )
| A、钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀 |
| B、原电池反应是导致金属腐蚀的主要原因,故不能用原电池原理来减缓金属的腐蚀 |
| C、钢铁电化学腐蚀的两种类型主要区别在于水膜的酸性不同,引起的正极反应不同 |
| D、无论哪种类型的腐蚀,其实质都是金属被氧化 |
下列说法不正确的是( )
| A、K+与Ar的结构示意图相同 |
B、二氧化碳的电子式: |
C、氧化钠的电子式: |
D、氯化氢的形成过程: |



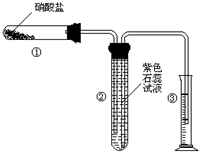 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)
某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出) 所含官能团的名称是
所含官能团的名称是