题目内容
下列有关的说法正确的是( )
| A、升高Fe2(SO4)3溶液的温度,其中水的离子积常数和pH均增加 |
| B、相同温度下1L 0.1mol.L-1NaF溶液跟1L 0.1mol.L-1NaCl溶液中所含离子总数不相等 |
| C、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液红色褪去,说明BaCl2溶液显酸性 |
| D、铅蓄电池放电时的负极和充电时的阴极匀发生还原反应 |
考点:盐类水解的原理,原电池和电解池的工作原理
专题:
分析:A、升高温度促进Fe2(SO4)3的水解,酸性增强,pH减小,
B、F-+H2O?HF+OH-,F-的物质的量等于OH-的物质的量,在H2O中c(H+)减少了;
C、碳酸钠水解呈碱性,加入氯化钡沉淀碳酸钡沉淀,导致水解平衡向逆向移动,据此解答;
D、充电时的阴极得电子发生还原反应.
B、F-+H2O?HF+OH-,F-的物质的量等于OH-的物质的量,在H2O中c(H+)减少了;
C、碳酸钠水解呈碱性,加入氯化钡沉淀碳酸钡沉淀,导致水解平衡向逆向移动,据此解答;
D、充电时的阴极得电子发生还原反应.
解答:
解:A、升高温度促进硫酸铁的水解,酸性增强,pH减小,故A错误;
B、F-+H2O?HF+OH-,F-的物质的量等于OH-的物质的量,但H2O中c(H+)减少了,所以等体积等物质的量浓度的NaF溶液与NaCl溶液中离子总数:N前<N后,故B正确;
C、碳酸钠水解呈碱性,加入氯化钡沉淀碳酸钡沉淀,导致水解平衡向逆向移动,溶液碱性减弱,故C错误;
D、负极失电子发生氧化反应,充电时的阴极得电子发生还原反应,故D错误;故选B.
B、F-+H2O?HF+OH-,F-的物质的量等于OH-的物质的量,但H2O中c(H+)减少了,所以等体积等物质的量浓度的NaF溶液与NaCl溶液中离子总数:N前<N后,故B正确;
C、碳酸钠水解呈碱性,加入氯化钡沉淀碳酸钡沉淀,导致水解平衡向逆向移动,溶液碱性减弱,故C错误;
D、负极失电子发生氧化反应,充电时的阴极得电子发生还原反应,故D错误;故选B.
点评:本题主要考查的数盐类水解的应用,涉及盐类水解的影响因素、离子浓度大小比较、原电池与电解池原理等,综合性较强,有一定难度.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
下列实验装置或操作正确的是( )
A、 烧杯中通入过量的CO2,出现白色沉淀,则溶液中一定含有AlO2- 烧杯中通入过量的CO2,出现白色沉淀,则溶液中一定含有AlO2- |
B、 装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
C、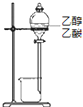 装置可以除去乙醇中的乙酸 装置可以除去乙醇中的乙酸 |
D、 装置可以比较碳酸钠、碳酸氢钠的热稳定性 装置可以比较碳酸钠、碳酸氢钠的热稳定性 |
 已知:NH2COO-+2H2O?HCO3-+NH3?H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )
已知:NH2COO-+2H2O?HCO3-+NH3?H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )| A、无法判断T1和T2的大小关系 |
| B、T1℃时,第6min反应物转化率为6.25% |
| C、T2℃时,0~6min ν(NH2COO-)=0.3mol?L-1?min-1 |
| D、往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小 |
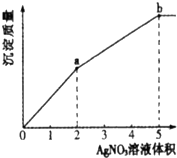 往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法正确的是( )
往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法正确的是( )| A、KSP(AgCl)<KSP(AgI) |
| B、c( Cl-):c( I-)=3:2 |
| C、m( AgCl ):m( AgI )=2:3 |
| D、a~b段产生黄色沉淀 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示,第三周中Z元素的简单离子半径最小,下列说法不正确( )
| X | Y | |||
| Z | W | Q |
| A、Y元素气态氢化物的稳定性大于X元素的气态氢化物 |
| B、形成的简单离子半径W>Q>Z>X |
| C、最高价氧化物对应的水化物酸性最强的是Q |
| D、X的最高价氧化物水化物和X的氢化物形成的化合物含有离子键,共价键 |
以KI为碘剂的加碘食盐,由于受空气作用,容易引起碘的损失,工业生产中需添加稳定剂以减少碘的损失.下列物质中可能做稳定剂的是( )
| A、Na2S2O3 |
| B、FeCl3 |
| C、NaHCO3 |
| D、CaO |
