题目内容
(1)含相同氧原子数的O2和O3的物质的量比 ,质量之比是 .
(2)有36克CO和CO2的混合气体在标准状况下体积为22.4L,则混合气体中CO的物质的量为 ,
(3)把VmL b mol/L的硫酸溶液;加水到体积为5VmL,则稀释后硫酸的物质的量浓度为 .
(4)1L K2SO4和MgSO4的混合溶液中,含Mg2+ 2.4g,SO
的物质的量浓度为1mol/L,则K2SO4的物质的量浓度是 .
(2)有36克CO和CO2的混合气体在标准状况下体积为22.4L,则混合气体中CO的物质的量为
(3)把VmL b mol/L的硫酸溶液;加水到体积为5VmL,则稀释后硫酸的物质的量浓度为
(4)1L K2SO4和MgSO4的混合溶液中,含Mg2+ 2.4g,SO
2- 4 |
考点:物质的量浓度的相关计算,物质的量的相关计算
专题:计算题
分析:(1)氧气和臭氧都只含有氧原子,如果氧原子数目相同,则二者的质量相等;物质的量与含有的氧原子的数目成反比;
(2)标准状况下,混合气体22.4L,物质的量为1mol,设CO的物质的量为x,CO2的物质的量为y,根据质量之和与物质的量之和列式计算可求得气体的物质的量,进而计算混合气体中CO的物质的量;
(3)稀释前后硫酸的物质的量不变,据此计算出稀释后的溶液中硫酸的浓度;
(4)根据n=
计算n(Mg2+),根据c=
计算出c(Mg2+),溶液中c(MgSO4)=c(Mg2+),溶液中c(SO42-)=c(MgSO4)+c(K2SO4),据此计算解答.
(2)标准状况下,混合气体22.4L,物质的量为1mol,设CO的物质的量为x,CO2的物质的量为y,根据质量之和与物质的量之和列式计算可求得气体的物质的量,进而计算混合气体中CO的物质的量;
(3)稀释前后硫酸的物质的量不变,据此计算出稀释后的溶液中硫酸的浓度;
(4)根据n=
| m |
| M |
| n |
| V |
解答:
解:(1)含相同氧原子数的O2和O3的物质的量比与分子中含有氧原子个数成反比,即:2:2,;由于氧气和臭氧分子中都只含有氧原子,则氧原子数目相同,其质量一定相等,
故答案为:3:2;1:1;
(2)标准状况下,混合气体22.4L的物质的量为1mol,
设CO的物质的量为x,CO2的物质的量为y,则:
x?28g/mol+y?44g/mol=36g,
x+y=1mol
解之得:x=0.5mol,y=0.5mol,
故答案为:0.5mol;
(3)稀释前后溶质硫酸的物质的量不变,则稀释后硫酸的物质的量浓度为:
=0.2bmol/L,
故答案为:0.2bmol/L;
(4)镁离子的物质的量为:n(Mg2+)=
=0.1mol,则c(Mg2+)=
=0.1mol/L,
溶液中c(MgSO4)=c(Mg2+)=0.1mol/L,(SO42-)=c(MgSO4)+c(K2SO4),
则c(K2SO4)=1mol/L-0.1mol/L=0.9mol/L,
故答案为:0.9mol/L.
故答案为:3:2;1:1;
(2)标准状况下,混合气体22.4L的物质的量为1mol,
设CO的物质的量为x,CO2的物质的量为y,则:
x?28g/mol+y?44g/mol=36g,
x+y=1mol
解之得:x=0.5mol,y=0.5mol,
故答案为:0.5mol;
(3)稀释前后溶质硫酸的物质的量不变,则稀释后硫酸的物质的量浓度为:
| bmol/L×V×10-3L |
| 5V×10-3L |
故答案为:0.2bmol/L;
(4)镁离子的物质的量为:n(Mg2+)=
| 2.4g |
| 24g/mol |
| 0.1mol |
| 1L |
溶液中c(MgSO4)=c(Mg2+)=0.1mol/L,(SO42-)=c(MgSO4)+c(K2SO4),
则c(K2SO4)=1mol/L-0.1mol/L=0.9mol/L,
故答案为:0.9mol/L.
点评:本题考查了物质的量、物质的量浓度的计算,题目难度中等,注意掌握物质的量、物质的量浓度的计算方法,(4)为易错点,注意明确各离子浓度之间的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 |
| B、配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 |
| C、Na2CO3溶液不可保存在带磨口塞的玻璃瓶中 |
| D、泡沫灭火器中常使用的原料是碳酸钠和硫酸铝 |
取100mL 2mol/L和300mL 1mol/L的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是( )
| A、1.5mol/L |
| B、2mol/L |
| C、1.0mol/L |
| D、1.6mol/L |
不影响H2O的电离平衡的粒子是( )
A、 | ||
B、
| ||
C、 | ||
D、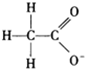 - - |
下列各项比较中正确的是( )
| A、微粒半径:Na+>S2->O2- |
| B、结合质子的能力:ClO->CH3COO->HCO3- |
| C、固体的热稳定性:Na2CO3>CaCO3>NaHCO3 |
| D、碱性:NaOH>KOH>Mg(OH)2 |
下列说法不正确的是( )
| A、SO2、Na2O2、活性炭都能使品红溶液褪色,但原理不同 |
| B、非金属氧化物不一定是酸性氧化物,但大多数金属氧化物为碱性氧化物 |
| C、强电解质在水中导电性一定大于弱电解质 |
| D、将40℃的饱和硫酸铜溶液升温至50℃,或者温度仍保持在40℃并加入少量无水硫酸铜,在这两种情况下溶液中溶质的质量分数均保持不变 |