题目内容
运用化学反应原理知识在工业生产中有重要意义.
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为 .
(2)工业生产中用CO可以合成甲醇
CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.

①p1 p2(填“大于”、“小于”或“等于”);
②100℃时,该反应的化学平衡常数K= (mol?L-1)-2;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率 (填“增大”、“减小”或“不变”).
(3)工业生产中用SO2为原料制取硫酸
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池的负极的电极反应式 .
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸.电解原理示意图如下图所示.请写出开始时阳极反应的电极反应式 .
(4)工业生产中用氨水吸收SO2若将等物质的量的SO2与NH3溶于水充分反应,写出该反应的离子方程式 ,所得溶液呈 性.
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为
(2)工业生产中用CO可以合成甲醇
CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.

①p1
②100℃时,该反应的化学平衡常数K=
③在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率
(3)工业生产中用SO2为原料制取硫酸
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池的负极的电极反应式
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸.电解原理示意图如下图所示.请写出开始时阳极反应的电极反应式
(4)工业生产中用氨水吸收SO2若将等物质的量的SO2与NH3溶于水充分反应,写出该反应的离子方程式
考点:热化学方程式,原电池和电解池的工作原理,化学平衡的影响因素
专题:化学反应中的能量变化,化学平衡专题,电化学专题
分析:(1)根据热化学方程式的含义和书写方法结合图中信息,利用盖斯定律来回答判断;
(2)①分析图象依据定一议二的方法分析,反应是气体体积减小的反应,温度一定,压强增大平衡正向进行,一氧化碳转化率增大;
②100°C时一氧化碳的转化率为0.5,结合化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,相当于增大压强,平衡正向进行,达到新平衡时一氧化碳转化率增大;
(3)①依据原电池原理,负极是失电子发生氧化反应,二氧化硫失电子生成硫酸的过程;
②根据化合价变化判断阳极反应物质,写出阳极反应式;
(4)工业生产中用氨水吸收SO2若将等物质的量的SO2与NH3溶于水充分反应生成亚硫酸氢铵,亚硫酸氢根离子电解大于水解溶液呈酸性.
(2)①分析图象依据定一议二的方法分析,反应是气体体积减小的反应,温度一定,压强增大平衡正向进行,一氧化碳转化率增大;
②100°C时一氧化碳的转化率为0.5,结合化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,相当于增大压强,平衡正向进行,达到新平衡时一氧化碳转化率增大;
(3)①依据原电池原理,负极是失电子发生氧化反应,二氧化硫失电子生成硫酸的过程;
②根据化合价变化判断阳极反应物质,写出阳极反应式;
(4)工业生产中用氨水吸收SO2若将等物质的量的SO2与NH3溶于水充分反应生成亚硫酸氢铵,亚硫酸氢根离子电解大于水解溶液呈酸性.
解答:
解:(1)第一步:2NH3(g)+CO2(g)?H2NCOONH4(l,氨基甲酸铵)△H1=-272KJ/mol,
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(s)△H2=138KJ/mol,
根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ?mol-1;
故答案为:2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ?mol-1;
(2)CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇;
①分析图象依据定一议二的方法分析,反应是气体体积减小的反应,温度一定,压强增大平衡正向进行,一氧化碳转化率增大,所以P1<P2;
故答案为:小于;
②100°C时一氧化碳的转化率为0.5,结合化学平衡三段式列式计算平衡浓度,
CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L)
0
变化量(mol/L)
平衡量(mol/L)
结合平衡常数概念计算得到;平衡常数K=
=(
)2(mol?L-1)-2;
故答案为:(
)2;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,相当于增大压强,平衡正向进行,达到新平衡时一氧化碳转化率增大;
故答案为:增大;
(3)①该原电池中,负极上失电子被氧化,二氧化硫到硫酸,硫的化合价升高,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,所以负极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,
故答案为:SO2-2e-+2H2O═SO42-+4H+;
②电解池中阳极和电源正极相连,失去电子,发生氧化反应,电解NaHSO3溶液可制得硫酸,硫的化合价升高,所以阳极是HSO3-溶液失去电子被氧化生成SO42-,则阳极电极反应式是:HSO3-+H2O-2e-=SO42-+3H+;
故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(4)用氨水吸收SO2若将等物质的量的SO2与NH3溶于水充分反应生成亚硫酸氢铵,反应的离子方程式为:SO2+NH3+H2O=NH4++HSO3-,亚硫酸氢根离子电解大于水解溶液呈酸性;
故答案为:SO2+NH3+H2O=NH4++HSO3-;酸.
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(s)△H2=138KJ/mol,
根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ?mol-1;
故答案为:2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ?mol-1;
(2)CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇;
①分析图象依据定一议二的方法分析,反应是气体体积减小的反应,温度一定,压强增大平衡正向进行,一氧化碳转化率增大,所以P1<P2;
故答案为:小于;
②100°C时一氧化碳的转化率为0.5,结合化学平衡三段式列式计算平衡浓度,
CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L)
| a |
| V |
| 2a |
| V |
变化量(mol/L)
| a |
| 2V |
| a |
| V |
| a |
| 2V |
平衡量(mol/L)
| a |
| 2V |
| a |
| V |
| a |
| 2V |
结合平衡常数概念计算得到;平衡常数K=
| ||||
|
| V |
| a |
故答案为:(
| V |
| a |
③在其它条件不变的情况下,再增加a mol CO和2a molH2,相当于增大压强,平衡正向进行,达到新平衡时一氧化碳转化率增大;
故答案为:增大;
(3)①该原电池中,负极上失电子被氧化,二氧化硫到硫酸,硫的化合价升高,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,所以负极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,
故答案为:SO2-2e-+2H2O═SO42-+4H+;
②电解池中阳极和电源正极相连,失去电子,发生氧化反应,电解NaHSO3溶液可制得硫酸,硫的化合价升高,所以阳极是HSO3-溶液失去电子被氧化生成SO42-,则阳极电极反应式是:HSO3-+H2O-2e-=SO42-+3H+;
故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(4)用氨水吸收SO2若将等物质的量的SO2与NH3溶于水充分反应生成亚硫酸氢铵,反应的离子方程式为:SO2+NH3+H2O=NH4++HSO3-,亚硫酸氢根离子电解大于水解溶液呈酸性;
故答案为:SO2+NH3+H2O=NH4++HSO3-;酸.
点评:本题考查了热化学方程式书写方法和盖斯定律计算应用,化学平衡影响因素分析判断,平衡常数计算,原电池原理和电解原理的应用,注意电极反应的书写方法,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
茫茫黑夜中,航标灯为航海员指明了方向.航标灯的电源必须长效、稳定.我国科技工作者研制出以铝、Pt-Fe合金网为电极材料的海水电池.在这种电池中①电子由外电路流向铝电极②铝是负极③海水是电解质溶液 ④铝电极发生还原反应,正确的是( )
| A、②③ | B、②④ | C、①② | D、①④ |
下列装置能构成原电池的是( )
A、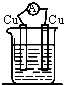 稀硫酸 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 无水乙醇 |
 由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下: