题目内容
10.在空气中长期放置的下列五种物质,易变质且发生的是氧化还原反应的是( )①氯水②亚硫酸钠③亚硫酸④氢硫酸⑤溴化银.
| A. | ①②③④ | B. | ①③④⑤ | C. | ①③④ | D. | 全部 |
分析 ①氯水中HClO易光照分解;
②亚硫酸钠、③亚硫酸中+4价S易被氧化;
④氢硫酸中-2价S易被氧化;
⑤溴化银易光照分解.
解答 解:①中发生2HClO $\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,为氧化还原反应,故选;
②发生2Na2SO3+O2═2Na2SO4,亚硫酸钠易被氧化为硫酸钠,为氧化还原反应,故选;
③发生2H2SO3+O2═2H2SO4,亚硫酸易被氧化为硫酸,为氧化还原反应,故选;
④氢硫酸发生2H2S+O2=2H2O+2S↓,为氧化还原反应,故选;
⑤溴化银发生2AgBr$\frac{\underline{\;光照\;}}{\;}$2Ag+Br2,为氧化还原反应,故选;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握物质的性质、发生的反应、元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
19.在容量瓶上无需标有( )
| A. | 刻度线 | B. | 容量标准 | C. | 浓度 | D. | 温度 |
18.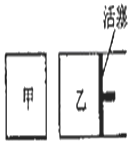 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2S03(g)并达到平衡.在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为b%,乙容器中SO2的转化率为a%,则a与b的关系为( )
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2S03(g)并达到平衡.在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为b%,乙容器中SO2的转化率为a%,则a与b的关系为( )
 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2S03(g)并达到平衡.在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为b%,乙容器中SO2的转化率为a%,则a与b的关系为( )
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2S03(g)并达到平衡.在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为b%,乙容器中SO2的转化率为a%,则a与b的关系为( )| A. | 无法确定 | B. | a<b | C. | a=b | D. | a>b |
5.游泳池是公共场合,必须保持用水的清洁卫生,游泳池中的水常用漂白粉消毒,漂白粉的有效成分是( )
| A. | CaCl2 | B. | Ca(ClO)2 | C. | Ca(OH)2 | D. | HClO |
15.下列物质的电子式或结构式书写正确的是( )
| A. | 氯化铵的电子式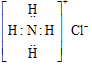 | B. | 氮气的电子式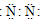 | ||
| C. | 次氯酸的结构式H-Cl-O | D. | 氯化钙的电子式 |
2.下列叙述正确的是( )
| A. | 若AgCl沉淀完全,就是指氯化银溶液中溶质离子的浓度为零 | |
| B. | 达到溶解平衡时,晶体就不再溶解 | |
| C. | 室温下,在100g水中能溶解1~10g的溶质,这种物质被称为可溶性物质 | |
| D. | 无机酸都是可溶的 |
19.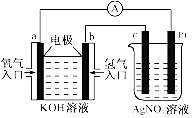 由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
 由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )| A. | 该装置中Pt极为阳极 | |
| B. | 当c极的质量变化了2.16g时,a极上消耗的O2在标准状况下的体积为1.12L | |
| C. | 该装置中b极的电极反应式是:H2+2OH--2e-=2H2O | |
| D. | 该装置中a极为正极,发生氧化反应 |
20.下列设计的实验方案能达到实验目的是( )
| A. | 探究H2O2溶液的氧化性:将H2O2溶液滴在淀粉碘化钾试纸上 | |
| B. | 验证醋酸是弱电解质:常温下测定0.1 mol•L-1CH3COONa溶液的pH | |
| C. | 比较铁与铜的还原性:常温下将铁片与铜片分别加入到浓HNO3中 | |
| D. | 检验溴元素:取少许CH3CH2Br与NaOH溶液共热,冷却后滴加AgNO3溶液 |