题目内容
5.已知下面热化学方程式:CH4(g)+2O2(g)=CO2 (g)+2H2O(l)△H=-890.36kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8k kJ•mol-1
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况下),在101kPa下经完全燃烧后恢复至常温,求放出的热量.
分析 标准状况下Vm=22.4L/mol,结合n=$\frac{V}{Vm}$及物质的量与热量成正比计算.
解答 解:n(混合气体)=$\frac{11.2L}{22.4L/mol}$=0.5mol,)
由此可得,n(CH4)=0.5mol×$\frac{4}{5}$=0.4mol、n(H2)=0.5mol×$\frac{1}{5}$=0.1mol,
设甲烷和氢气燃烧放出的热量分别为x和y,则
CH4(g)+2O2(g)=CO2 (g)+2H2O(l)△H=-890.36 kJ•mol-1
1 890.36
0.4mol x
$\frac{1}{0.4}=\frac{890.36}{x}$,解得:x=356.144kJ,
H2(g)+1/2O2(g)=H2O(l)△H=-285.8k kJ•mol-1
1 285.8
0.1mol y
$\frac{1}{0.1}=\frac{285.8}{y}$,解得:y=28.58kJ,
反应放出的总热量Q(总)=356.144kJ+28.58kJ=384.724kJ,
答:完全燃烧后恢复至常温放出的热量为384.724kJ.
点评 本题考查热化学反应方程式的计算,为高频考点,把握物质的量与热量的关系为解答的关键,侧重分析与计算能力的考查,注意常温下水为液态,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 通常状况(室温、101kP)下,气体摩尔体积约为22.4L/mol | |
| C. | 标准状况(0℃、101kP)下,气体摩尔体积约为22.4 L | |
| D. | 标准状况(0℃、101kP)下,1 mol H2O的体积是22.4 L |
①Fe+Cu2+═Fe2++Cu ②Ba2++OH-+H++SO42-═BaSO4↓+H2O
③Ba2++OH-+H++SO42-═BaSO4↓+2H2O ④Cl2+H2O═H+Cl-+HClO
⑤CO32-+2H+═CO2+H2O ⑥Ag++Cl-═AgCl↓
| A. | ①②⑤⑥ | B. | ①②③⑤⑥ | C. | ③④ | D. | 只有④ |
| A. | ${\;}_{6}^{12}$C与${\;}_{6}^{14}$C互为同位素 | B. | 乙烯分子的结构简式:CH2=CH2 | ||
| C. | 氟离子结构示意图: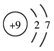 | D. | -OH的电子式: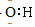 |
| A. | 在平衡常数表达式中,反应物浓度用起始浓度,生成物用平衡浓度 | |
| B. | 在任何条件下,化学平衡常数是一个恒定值 | |
| C. | 平衡常数的大小只与温度有关,而与浓度、催化剂等无关 | |
| D. | 改变压强,化学平衡常数不一定发生改变 |
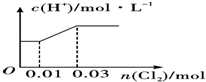

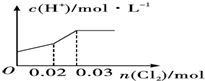
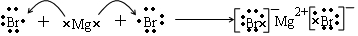 .
.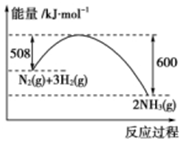 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式: