题目内容
13.下列物质:①Fe ②O2③Na2O ④NH3 ⑤CO2 ⑥蔗糖 ⑦NaCl ⑧稀盐酸 ⑨H2SO4 ⑩BaSO4属于电解质的是③⑦⑨⑩,属于非电解质的有④⑤⑥(用序号填写).分析 水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质也不是非电解质.
解答 解:①Fe②O2是金属单质,既不是电解质也不是非的电解质;
③Na2O熔融状态下能导电,属于电解质;
④NH3溶于水因为生成了一水合氨,本身不能电离,属于非电解质;
⑤CO2溶于水能导电是因为生成了亚硫酸,本身不能电离,属于非电解质;
⑥蔗糖不能导电,属于非电解质;
⑦NaCl溶于水能导电,属于电解质;
⑧稀盐酸属于混合物,既不是电解质也不是非的电解质;
⑨H2SO4 溶于水能导电,属于电解质;
⑩硫酸钡固体不能导电,熔融状态下能导电,属于电解质,
所以属于电解质的是③⑦⑨⑩,属于非电解质的有④⑤⑥;
故答案为:③⑦⑨⑩;④⑤⑥.
点评 本题考查了电解质与非电解质的判断、物质的分类方法,题目难度不大,注意掌握电解质与非电解质的概念及判断方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.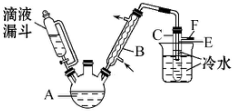 某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:
某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:
乙醇、溴乙烷、溴有关参数
(1)制备操作中,加入的浓硫酸必须进行稀释,其目的是abc( 多选 ).
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发d.水是反应的催化剂
(2)写出溴化氢与浓硫酸加热时发生反应的化学方程式2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$SO2+Br2+2H2O.
(3)加热的目的是加快反应速率,蒸馏出溴乙烷.
(4)图中试管C中的导管E的末端必须在水面以下,其原因是通过冷却得到溴乙烷,减少溴乙烷的挥发.
(5)为除去产品中的一种主要杂质,最好选择下列D(选填序号)溶液来洗涤产品.
A.氢氧化钠 B.氯化钠
C.碘化亚铁 D.亚硫酸钠
(6)第(5)题的实验所需要的玻璃仪器有分液漏斗、烧杯.
 某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:
某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必须进行稀释,其目的是abc( 多选 ).
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发d.水是反应的催化剂
(2)写出溴化氢与浓硫酸加热时发生反应的化学方程式2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$SO2+Br2+2H2O.
(3)加热的目的是加快反应速率,蒸馏出溴乙烷.
(4)图中试管C中的导管E的末端必须在水面以下,其原因是通过冷却得到溴乙烷,减少溴乙烷的挥发.
(5)为除去产品中的一种主要杂质,最好选择下列D(选填序号)溶液来洗涤产品.
A.氢氧化钠 B.氯化钠
C.碘化亚铁 D.亚硫酸钠
(6)第(5)题的实验所需要的玻璃仪器有分液漏斗、烧杯.
1.下列说法正确的是( )
| A. | 常温下,PH=9的碳酸钠溶液中由水电离出的c(OH-)=1×10-9mol•L-1 | |
| B. | 饱和氯水中:c(Cl-)=c(ClO-)+c(HClO) | |
| C. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| D. | 中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1 |
8.室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,其过程表示为:
CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l) 热效应为△H1;将 1mol CuSO4(s)溶于水会使溶液温度升高,其过程表示为:CuSO4(s)=Cu2+(aq)+SO42-(aq) 热效应为△H2;CuSO4•5H2O受热分解的化学方程式为:CuSO4•5H2O(s) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4(s)+5H2O(l),热效应为△H3.则下列判断正确的是( )
CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l) 热效应为△H1;将 1mol CuSO4(s)溶于水会使溶液温度升高,其过程表示为:CuSO4(s)=Cu2+(aq)+SO42-(aq) 热效应为△H2;CuSO4•5H2O受热分解的化学方程式为:CuSO4•5H2O(s) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4(s)+5H2O(l),热效应为△H3.则下列判断正确的是( )
| A. | △H1<△H3 | B. | △H2>△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2>△H3 |
2.在下列反应中,水既不是氧化剂,也不是还原剂的是( )
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | C12+H2O=HC1+HC1O | ||
| C. | 2F2+2H2O=4HF+O2 | D. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
13.下列可逆反应达到平衡后,加压或升高温度可使平衡向逆反应方向移动的是( )
| A. | A2(g)+B2(g)?2AB(g)△H<0 | B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | ||
| C. | W(g)?Z(g)△H<0 | D. | 2SO3(g)?2SO2(g)+O2(g)△H>0 |