题目内容
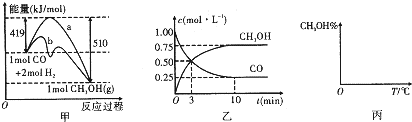
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).如图中甲图表示反应过程中能量的变化情况;乙图表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间的变化情况.
请回答下列问题.
(1)下列说法正确的是 (填字母序号).
a.在甲图中,曲线b表示使用了催化剂
b.起始充入的CO为2mol,从反应开始到达到平衡,v(H2)=0.075mol?L-1?min-1,
c.增大CO的浓度,CO的转化率增大
d.容器中压强恒定时,说明反应已达平衡状态
e.保持温度和密闭容器的容积不变,再充入1mol CO和2mol H2,再次达到平衡时
的值会变小
(2)该温度下CO(g)+2H2 (g)?CH3OH(g)的化学平衡常数为 .若保持其他条件不变,将反应体系升温,则该反应的化学平衡常数 (填“增大”“减小”或“不变”).
(3)请在丙图所示坐标图中画出平衡时甲醇的百分含量(纵坐标)随温度(横坐标)的变化曲线,要求画出压强不同的两条曲线(在曲线上标出P1、P2且P1<P2).
(4)已知CH3OH(g)+
O2(g)═C02(g)+2H2O(g)△H=-192.9kJ/mol,又知H20(1)═H2O(g)△H=+44kJ/mol,请写出32g CH3OH(g)完全燃烧生成CO2和液态水的热化学方程式 .

请回答下列问题.
(1)下列说法正确的是
a.在甲图中,曲线b表示使用了催化剂
b.起始充入的CO为2mol,从反应开始到达到平衡,v(H2)=0.075mol?L-1?min-1,
c.增大CO的浓度,CO的转化率增大
d.容器中压强恒定时,说明反应已达平衡状态
e.保持温度和密闭容器的容积不变,再充入1mol CO和2mol H2,再次达到平衡时
| n(CH3OH) |
| n(CO) |
(2)该温度下CO(g)+2H2 (g)?CH3OH(g)的化学平衡常数为
(3)请在丙图所示坐标图中画出平衡时甲醇的百分含量(纵坐标)随温度(横坐标)的变化曲线,要求画出压强不同的两条曲线(在曲线上标出P1、P2且P1<P2).
(4)已知CH3OH(g)+
| 3 |
| 2 |
考点:物质的量或浓度随时间的变化曲线,热化学方程式,化学平衡的影响因素
专题:基本概念与基本理论
分析:(1)①a、在甲图中,曲线b表示使用了催化剂,反应的活化能降低;
b、起始充入的CO为2mol,说明容器体积为2L,v(CO)=
mol?L-1?min-1,所以v(H2)=2v(CO)=0.15mol?L-1?min-1;
c、增加CO浓度,会促进氢气的转化,但本身的转化率降低;
d、该反应为反应前后压强不等的反应;
e、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,比值增大;
(2)利用各物质平衡的浓度来计算化学平衡常数;根据温度升高,平衡逆向移动,平衡常数减小;
(3)该反应为放热反应,升高温度甲醇含量减小,增大压强甲醇含量增大;
(4)根据盖斯定律和已知热化学方程式来构建目标化学方程式并求出反应热.
b、起始充入的CO为2mol,说明容器体积为2L,v(CO)=
| 1-0.25 |
| 10 |
c、增加CO浓度,会促进氢气的转化,但本身的转化率降低;
d、该反应为反应前后压强不等的反应;
e、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,比值增大;
(2)利用各物质平衡的浓度来计算化学平衡常数;根据温度升高,平衡逆向移动,平衡常数减小;
(3)该反应为放热反应,升高温度甲醇含量减小,增大压强甲醇含量增大;
(4)根据盖斯定律和已知热化学方程式来构建目标化学方程式并求出反应热.
解答:
解:(1)a、在甲图中,曲线b表示使用了催化剂,反应的活化能降低,故选;
b、起始充入的CO为2mol,说明容器体积为2L,v(CO)=
mol?L-1?min-1,所以v(H2)=2v(CO)=0.15mol?L-1?min-1,故不选;
c、增加CO浓度,会促进氢气的转化,但本身的转化率降低,故不选;
d、该反应为反应前后压强不等的反应,容器中压强恒定时,说明反应已达平衡状态,故选;
e、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,比值增大,故不选;
故答案为:ad;
(2)CO(g)+2H2(g)?CH3OH(g)
开始(mol/L) 1 2 0
转化(mol/L) 0.75 1.5 0.75
平衡(mol/L) 0.25 0.5 0.75
则化学平衡常数K=
=12;温度升高,平衡逆向移动,反应物的浓度增大,生成物的浓度减少,平衡常数减小;
故答案为:12;减小;
(3)该反应为放热反应,因温度升高,平衡逆向移动,反应物的浓度增大,生成物的浓度减少,温度相同时压强越大,CH3OH的百分含量越高,所以图为: ,故答案为:
,故答案为: ;
;
(4)32g的CH3OH(g)即为1mol,
则H3OH(g)+
O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol ①
H2O(l)=H2O(g)△H=+44kJ/mol ②
根据盖斯定律①-②×2得 CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-280.9kJ/mol
故答案为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-280.9kJ/mol.
b、起始充入的CO为2mol,说明容器体积为2L,v(CO)=
| 1-0.25 |
| 10 |
c、增加CO浓度,会促进氢气的转化,但本身的转化率降低,故不选;
d、该反应为反应前后压强不等的反应,容器中压强恒定时,说明反应已达平衡状态,故选;
e、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,比值增大,故不选;
故答案为:ad;
(2)CO(g)+2H2(g)?CH3OH(g)
开始(mol/L) 1 2 0
转化(mol/L) 0.75 1.5 0.75
平衡(mol/L) 0.25 0.5 0.75
则化学平衡常数K=
| 0.75 |
| 0.25×0.5×0.5 |
故答案为:12;减小;
(3)该反应为放热反应,因温度升高,平衡逆向移动,反应物的浓度增大,生成物的浓度减少,温度相同时压强越大,CH3OH的百分含量越高,所以图为:
 ,故答案为:
,故答案为: ;
;(4)32g的CH3OH(g)即为1mol,
则H3OH(g)+
| 3 |
| 2 |
H2O(l)=H2O(g)△H=+44kJ/mol ②
根据盖斯定律①-②×2得 CH3OH(g)+
| 3 |
| 2 |
故答案为:CH3OH(g)+
| 3 |
| 2 |
点评:本题考查化学平衡状态判断、化学平衡有关计算、影响化学平衡的因素、化学平衡图象、盖斯定律的应用等,题目难度中等,侧重于考查学生对所学知识的综合应用能力,注意把握三段式在化学平衡计算中的应用.

练习册系列答案
相关题目
在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:2R(气)+5Q(气)=3X(气)+nY(气)反应完全后,容器温度不变,混和气体的压强是原来的97.5%,则化学方程式中的n值是( )
| A、3 | B、4 | C、5 | D、6 |
下列说法错误的是( )
| A、FeS不溶于水,但能溶于稀硫酸中 |
| B、CaCO3难溶于稀硫酸,也难溶于醋酸中 |
| C、洗涤沉淀时用水洗涤造成的BaSO4损失量大于用稀硫酸洗涤的损失量 |
| D、某离子被沉淀完全,但该离子在溶液中的浓度不为0 |
绿原酸是咖啡的热水提取液成分之一,结构简式如图,关于绿原酸判断正确的是( )

| A、分子中所有的碳原子均可能在同一平面内 |
| B、1 mol绿原酸与足量溴水反应,最多消耗2.5 mol Br2 |
| C、1 mol绿原酸与足量NaOH溶液反应,最多消耗4 mol NaOH |
| D、绿原酸水解产物均可以与FeCl3溶液发生显色反应 |
 已知NaCl的摩尔质量为58.5g.mol-1,食盐晶体的密度为ρ.gcm-3,若如图中Na+与最邻近Cl-的核间距离为acm,那么阿伏加德罗常数可表示为( )
已知NaCl的摩尔质量为58.5g.mol-1,食盐晶体的密度为ρ.gcm-3,若如图中Na+与最邻近Cl-的核间距离为acm,那么阿伏加德罗常数可表示为( )A、
| ||
B、
| ||
C、
| ||
| D、117a3ρ |
以下都是常见的抗酸剂,对于胃溃疡较重的病人,不适合使用的抑酸剂是( )
| A、Mg(OH)2 |
| B、Al(OH)3 |
| C、NaHCO3 |
| D、三硅酸镁(2MgO?3SiO2?nH2O) |
下列说法不正确的是( )
| A、医用酒精的浓度通常为95% |
| B、氯气易液化,可用钢瓶储存液氯 |
| C、天然橡胶、聚氯乙烯的链节中均含有两种官能团 |
| D、向某溶液加入CCl4,若CCl4层显橙红色,证明原溶液中存在Br2 |