题目内容
(1)下列根据实验事实得出的结论,正确的有 (填序号)
①试液
颜色无变化
溶液变为血红色
结论:试液中含有Fe2+
②试液
白色沉淀
沉淀不溶解
结论:试液中含有SO42-
③Ba(OH)2溶液
溶液的导电能力先减弱后增强
结论:Ba(OH)2和H2SO4之间的反应是离子反应
④稀硫酸
产生少量气泡
产生大量气泡,
结论:CuSO4是锌与稀硫酸反应的催化剂
(2)现有三位同学分别利用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制取少量漂白粉,设计了三套实验装置:
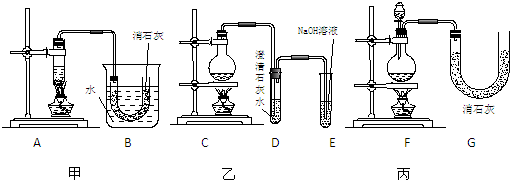
已知:温度稍高即发生如下副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O
1.请写出制备氯气时发生反应的化学反应方程式,并用单线桥法表示出电子转移.
2.三位同学所设计的装置都有优点和缺点,请从你的角度分析甲同学装置的优缺点.优点: .
缺点: .请从上述装置的A-G的组成中选取合理的部分组装一套较完善的实验装置,装置各部分的连接顺序(按气流从左到右的方向)是 .
3.近几年欧美发达国家使用了一种更安全、高效的杀菌消毒物质二氧化氯.它对水中的重金属离子和氰化物都有很高的去除效果.二氧化氯可以将氰化物转化成两种空气成分气体.请写出过程中所发生反应的离子方程式: .
①试液
| KSCN溶液 |
| H2O2溶液 |
结论:试液中含有Fe2+
②试液
| BaCl2溶液 |
| 稀HNO3 |
结论:试液中含有SO42-
③Ba(OH)2溶液
| 逐滴加入稀硫酸 |
结论:Ba(OH)2和H2SO4之间的反应是离子反应
④稀硫酸
| 纯锌片 |
| CuSO4溶液 |
结论:CuSO4是锌与稀硫酸反应的催化剂
(2)现有三位同学分别利用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制取少量漂白粉,设计了三套实验装置:

已知:温度稍高即发生如下副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O
1.请写出制备氯气时发生反应的化学反应方程式,并用单线桥法表示出电子转移.
2.三位同学所设计的装置都有优点和缺点,请从你的角度分析甲同学装置的优缺点.优点:
缺点:
3.近几年欧美发达国家使用了一种更安全、高效的杀菌消毒物质二氧化氯.它对水中的重金属离子和氰化物都有很高的去除效果.二氧化氯可以将氰化物转化成两种空气成分气体.请写出过程中所发生反应的离子方程式:
考点:物质的检验和鉴别的基本方法选择及应用,氯、溴、碘的性质实验
专题:
分析:(1)①亚铁离子不能使KSCN溶液变红色,铁离子可以使KSCN溶液变红色;
②检验硫酸根离子应该先将盐酸,再加氯化钡溶液;
③Ba(OH)2溶液与稀硫酸反应生成硫酸钡沉淀;
④形成原电池能加快反应速率;
(2)1、二氧化锰与浓盐酸反应生成氯气、氯化锰和水,根据化合价的变化分析电子转移;
2、甲同学的装置有冷却装置,没有用分液漏斗,没有尾气处理装置;组装一套较完善的实验装置,则需要能控制反应速率的装置、冷却装置、尾气处理装置;
3、用ClO2氧化除去CN-,生成二氧化碳和氮气等无毒气体.
②检验硫酸根离子应该先将盐酸,再加氯化钡溶液;
③Ba(OH)2溶液与稀硫酸反应生成硫酸钡沉淀;
④形成原电池能加快反应速率;
(2)1、二氧化锰与浓盐酸反应生成氯气、氯化锰和水,根据化合价的变化分析电子转移;
2、甲同学的装置有冷却装置,没有用分液漏斗,没有尾气处理装置;组装一套较完善的实验装置,则需要能控制反应速率的装置、冷却装置、尾气处理装置;
3、用ClO2氧化除去CN-,生成二氧化碳和氮气等无毒气体.
解答:
解:(1)①亚铁离子不能使KSCN溶液变红色,铁离子可以使KSCN溶液变红色,试液
颜色无变化
溶液变为血红色,说明原溶液中含有Fe2+,故正确;
②检验硫酸根离子应该先将盐酸,再加氯化钡溶液,不能加硝酸,因为硝酸能把亚硫酸根离子氧化为硫酸根离子,故错误;
③Ba(OH)2溶液中加热稀硫酸反应生成硫酸钡沉淀,溶液中离子浓度减小,则导电性减弱,当硫酸过量时,溶液中离子浓度又增大,则溶液的导电性增强,所以Ba(OH)2溶液
溶液的导电能力先减弱后增强,结论:Ba(OH)2和H2SO4之间的反应是离子反应,故正确;
④稀硫酸
产生少量气泡
产生大量气泡,Zn、Cu与稀硫酸形成原电池能加快反应速率,故错误;
故答案为:①④;
(2)1、二氧化锰与浓盐酸反应生成氯气、氯化锰和水,反应中4molHCl中有2molHCl失去2mol电子,而1mol二氧化锰恰好得到2mol电子,用单线桥法表示出电子转移为: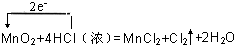 ,故答案为:
,故答案为: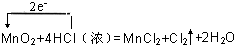 ;
;
2、用Cl2和Ca(OH)2反应制取少量漂白粉时,温度稍高即发生副反应,甲同学的装置中用水冷却可以防止发生副反应,没有使用分液漏斗,不容易控制反应速率,氯气为有毒气体,应该加一个尾气处理装置;若组装一套较完善的实验装置,则需要能控制反应速率的装置、冷却装置、尾气处理装置,则仪器连接顺序为F→B→E;
故答案为:可防止副反应发生;不容易控制反应速率、污染环境;F→B→E;
3、用ClO2氧化除去CN-,生成二氧化碳和氮气等无毒气体,离子反应为2ClO2+2CN-=2CO2↑+N2↑+2Cl-,故答案为:2ClO2+2CN-=2CO2↑+N2↑+2Cl-.
| KSCN溶液 |
| H2O2溶液 |
②检验硫酸根离子应该先将盐酸,再加氯化钡溶液,不能加硝酸,因为硝酸能把亚硫酸根离子氧化为硫酸根离子,故错误;
③Ba(OH)2溶液中加热稀硫酸反应生成硫酸钡沉淀,溶液中离子浓度减小,则导电性减弱,当硫酸过量时,溶液中离子浓度又增大,则溶液的导电性增强,所以Ba(OH)2溶液
| 逐滴加入稀硫酸 |
④稀硫酸
| 纯锌片 |
| CuSO4溶液 |
故答案为:①④;
(2)1、二氧化锰与浓盐酸反应生成氯气、氯化锰和水,反应中4molHCl中有2molHCl失去2mol电子,而1mol二氧化锰恰好得到2mol电子,用单线桥法表示出电子转移为:
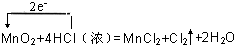 ,故答案为:
,故答案为: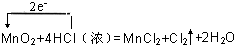 ;
;2、用Cl2和Ca(OH)2反应制取少量漂白粉时,温度稍高即发生副反应,甲同学的装置中用水冷却可以防止发生副反应,没有使用分液漏斗,不容易控制反应速率,氯气为有毒气体,应该加一个尾气处理装置;若组装一套较完善的实验装置,则需要能控制反应速率的装置、冷却装置、尾气处理装置,则仪器连接顺序为F→B→E;
故答案为:可防止副反应发生;不容易控制反应速率、污染环境;F→B→E;
3、用ClO2氧化除去CN-,生成二氧化碳和氮气等无毒气体,离子反应为2ClO2+2CN-=2CO2↑+N2↑+2Cl-,故答案为:2ClO2+2CN-=2CO2↑+N2↑+2Cl-.
点评:本题考查了物质的检验、离子反应、原电池原理的应用、物质制备实验方案的设计等,题目难度中等,侧重于考查学生对基础知识的应用能力和实验探究能力.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
 如图是某学生设计的制取和收集某些气体的实验装置(可加热).
如图是某学生设计的制取和收集某些气体的实验装置(可加热).