题目内容
下列叙述错误的是( )
| A、1mol任何粒子集体都含有约6.02×1023个该种粒子 |
| B、0.012kg12C 含有约6.02×1023个碳原子 |
| C、1mol水中含有2mol氢元素和1mol氧元素 |
| D、1molNH3约含有6.02×1024个电子 |
考点:阿伏加德罗常数,物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据阿伏伽德罗常数的概念分析判断,1mol任何微粒集体含有阿伏伽德罗常数个微粒;
B、依据规定0.012kg12C 含有碳原子数为1mol分析;
C、物质的量 是描述微观粒子的物理量,元素是宏观概念;
D、1molNH3约含10mol电子分析;
B、依据规定0.012kg12C 含有碳原子数为1mol分析;
C、物质的量 是描述微观粒子的物理量,元素是宏观概念;
D、1molNH3约含10mol电子分析;
解答:
解:A、依据阿伏伽德罗常数的概念分析判断,1mol任何微粒集体含有阿伏伽德罗常数个微粒,1mol任何粒子集体都含有约6.02×1023个该种粒子,故A正确;
B、依据规定0.012kg12C 含有碳原子数为1mol,0.012kg12C 含有约6.02×1023个碳原子,故B正确;
C、物质的量 是描述微观粒子的物理量,元素是宏观概念,1mol水中含有2mol氢原子和1mol氧原子,故C错误;
D、1molNH3约含10mol电子,约含有6.02×1024个电子,故D正确;
故选C.
B、依据规定0.012kg12C 含有碳原子数为1mol,0.012kg12C 含有约6.02×1023个碳原子,故B正确;
C、物质的量 是描述微观粒子的物理量,元素是宏观概念,1mol水中含有2mol氢原子和1mol氧原子,故C错误;
D、1molNH3约含10mol电子,约含有6.02×1024个电子,故D正确;
故选C.
点评:本题考查阿伏伽德罗常数的分析应用,主要是常数的规定,物质的量概念的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
 已知芳香烃A、B的结构模型如图所示,相关叙述错误的是( )
已知芳香烃A、B的结构模型如图所示,相关叙述错误的是( )A、A的结构简式为 |
| B、A中有两种不同类型的碳碳键 |
| C、B与A为同系列物质,通式为C6nH4n+2(n为苯环数) |
| D、与B互为同类别的同分异构体共有3种 |
同周期的三种元素X、Y、Z,已知它们的最高价氧化物对应的水化物的碱性由强到弱的顺序为 XOH>Y(OH)2>Z(OH)3,则下列叙述中正确的是( )
| A、原子的失电子能力 X>Y>Z |
| B、X、Y、Z的单质与水反应是越来越容易 |
| C、原子半径 Z>Y>X |
| D、原子序数X>Y>Z |
高铁电池是电动汽车首选的电池之一,该电池的工作原理为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是( )
| 放电 |
| 充电 |
| A、高铁电池产生的电流从负极经外电路到达正极 |
| B、正极反应式为Zn+2OH--2e-═Zn(OH)2 |
| C、负极pH减小,正极pH增大,电解液pH增大 |
| D、每氧化1mol高铁酸钾转移3mol电子 |
可以用于除去氯气中水蒸气的干燥剂是( )
| A、碱石灰 | B、浓硫酸 |
| C、生石灰 | D、固体烧碱 |
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则( )
| A、原子半径:丙<丁<乙 |
| B、乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
| C、甲、乙、丙的氧化物均为共价化合物 |
| D、单质的还原性:丁>丙>甲 |
近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为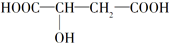 ,下列说法不正确的是( )
,下列说法不正确的是( )
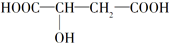 ,下列说法不正确的是( )
,下列说法不正确的是( )| A、苹果酸在一定条件下能发生酯化反应 |
| B、苹果酸在一定条件下能发生催化氧化反应 |
| C、苹果酸1 mol能与3 mol Na反应 |
| D、1 mol苹果酸与Na2CO3溶液反应最多消耗3 mol Na2CO3 |




 物质X、Y、Z均含同种短周期元素,其转化关系如图所示(反应条件未标出).
物质X、Y、Z均含同种短周期元素,其转化关系如图所示(反应条件未标出).