题目内容
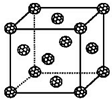
16.下列实验操作中,正确的是( ) |  |  |  |
| A.将NaOH溶液存 放在玻璃瓶中 | B.检验试液中NH4+ 的存在 | C.干燥CO2气体 | D.收集HCl气体 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.应利用橡皮塞存放;
B.生成的氨气,能使红色石蕊试纸变蓝;
C.CO2与碱石灰反应;
D.HCl极易溶于水.
解答 解:A.应利用橡皮塞存放,不能利用胶头滴管将NaOH溶液存放在玻璃瓶中,故A错误;
B.生成的氨气,能使红色石蕊试纸变蓝,则图中可检验试液中NH4+的存在,故B正确;
C.CO2与碱石灰反应,不能干燥CO2,故C错误;
D.HCl极易溶于水,不能利用图中排水法收集,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握实验基本操作及物质性质为解答的关键,侧重实验基本知识和物质检验、气体收集的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
6.将20.8g Cu和CuO的混合物加入到1L混有H2SO4的Fe2(SO4)3溶液中,样品完全溶解时,溶液中Fe3+、Fe2+、H+的物质的量之比为1:4:1(不考虑溶液体积的变化).若测得反应后溶液中的c(H+)=0.1mol•L-1,则下列说法中错误的是( )
| A. | 原混合物中Cu为12.8g | B. | 原溶液中c(SO42-)=0.15mol•L-1 | ||
| C. | 反应后溶液中Cu2+为0.3mol | D. | 反应后溶液中c(SO42-)为0.8mol•L-1 |
7.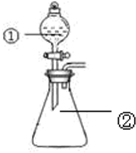 用如图所示装置进行下列实验:将①中溶液滴入②锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②锥形瓶中,预测的现象与实际相符的是( )
 用如图所示装置进行下列实验:将①中溶液滴入②锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②锥形瓶中,预测的现象与实际相符的是( ) | 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D. | SO2饱和溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
11.下列关于元素周期律的说法中错误的是( )
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 离子的还原性:S2->Cl->Br->I- | |
| C. | 酸性:H2SO4>H3PO4>H2CO3>HClO | |
| D. | 金属性:Be<Mg<Ca<K |
8.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能自发进行 | |
| C. | 反应物和生成物所具有的总焓决定了反应是放热还是吸热 | |
| D. | 放热反应在任何条件下也能发生反应 |
5.下列反应的离子方程式表示正确的是( )
| A. | 澄清石灰水中通入过量二氧化碳:OH-+CO2═HCO3- | |
| B. | 向水玻璃中中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
6.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2 L Cl2含有的分子数为0.5NA | |
| B. | 在常温常压下,17 g NH3所含的原子数为4NA | |
| C. | 标准状况下,11.2 L CCl4所含的分子数为0.5NA | |
| D. | 56g金属铁与足量的氯气反应时,失去的电子数为2NA |