题目内容
将5mol/L的AlCl3溶液a mL稀释至b mL,稀释后溶液中Cl-物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:
分析:根据稀释溶液浓度公式c1?V1=c2?V2计算即可.
解答:
解:稀释前氯离子浓度c1=5mol/L×3=15mol/L,则稀释后的氯离子浓度c2=
=
=
mol/L.故选B.
| c1?v1 |
| v2 |
| 15mol/L?a×10-3L |
| b×10-3L |
| 15a |
| b |
点评:本题考查了物质的量浓度的计算,注意AlCl3溶液浓度和氯离子浓度的关系,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
现代人正进入以“室内空气污染”为标志的第三个污染时期?以下不属于室内空气污染的是( )
| A、烹饪时产生的油烟 |
| B、二氧化碳含量过高造成的温室效应 |
| C、石材释放出的放射性有害气体 |
| D、劣质黏合剂释放出的甲醛等有害物质 |
下列能用勒沙特列原理解释的是( )
①红棕色NO2加压后颜色先变深后变浅
②SO2催化氧化成SO3的反应,往往加入过量的空气
③Fe(SCN)3溶液中加入固体KSCN后颜色变深
④氯水宜保存在低温、避光条件下
⑤乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利.
①红棕色NO2加压后颜色先变深后变浅
②SO2催化氧化成SO3的反应,往往加入过量的空气
③Fe(SCN)3溶液中加入固体KSCN后颜色变深
④氯水宜保存在低温、避光条件下
⑤乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利.
| A、①②⑤ | B、②③④ |
| C、①②③⑤ | D、全部 |
下列说法合理的是( )
| A、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B、由水溶液的酸性:HCI>H2S,可推断出元素的非金属性:CI>S |
| C、邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键 |
| D、H-F、H-O、H-N三种共价键的极性逐渐增强 |
有关化学用语的表示正确的是( )
| A、HCN分子的结构式:H-C≡N |
B、二氧化碳的电子式: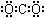 |
C、Cl-的结构示意图为: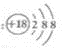 |
| D、乙烯的结构简式为CH2CH2 |
科学家发现一种化学式为O4的氧分子.1mol O3和1mol O4具有相同的( )
| A、分子数 | B、原子数 |
| C、质子数 | D、电子数 |
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- | ||||
B、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| C、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- | ||||
| D、稀硫酸滴在铜片上:Cu+2H+→Cu2++H2↑ |
下列关于化学变化的说法中,错误的是( )
| A、化学键断裂时要吸收能量,形成新化学键时要放出能量 |
| B、化学变化的实质是旧化学键断裂,新化学键形成 |
| C、在化学变化过程中,一定要吸收或放出能量 |
| D、吸收能量或放出能量的过程,一定是化学变化过程 |