题目内容
某样品中含有碳酸钠及少量的硫酸钠和氯化钠.某同学为了检验其成分,按照下列步骤进行实验,请将所加试剂及有关结论填写在相应的空格中.
向样品溶液中加入过量的 ,产生能使澄清石灰水变浑浊的气体,说明溶液中含有 .继续向溶液中加入过量的 ,产生白色沉淀,说明溶液中含有 .过滤,向滤液中加入 ,产生白色沉淀,说明溶液中含有 .
向样品溶液中加入过量的
考点:钠的重要化合物
专题:元素及其化合物
分析:检验样品中含有碳酸钠及少量的硫酸钠和氯化钠,先加硝酸排除碳酸钠的干扰,再用硝酸钡检验硫酸钠,最后用硝酸银和稀硝酸检验氯离子,故检验顺序为碳酸钠、硫酸钠、氯化钠,以此来解答.
解答:
解:检验样品中含有碳酸钠及少量的硫酸钠和氯化钠,先加过量HNO3溶液排除碳酸钠的干扰,同时检验碳酸钠的存在,再用过量Ba(NO3)溶液检验硫酸钠生成白色沉淀,最后用少量AgNO3溶液检验氯离子生成白色沉淀,所以可依次检验出Na2CO3、Na2SO4、NaCl,
故答案为:硝酸; 碳酸钠;硝酸钡;硫酸钠;硝酸银;氯化钠;
故答案为:硝酸; 碳酸钠;硝酸钡;硫酸钠;硝酸银;氯化钠;
点评:本题考查物质鉴别和检验实验,为高频考点,本题注意Cl-、SO42-的性质,把握除杂原则,提纯时不能引入新的杂质,注意把握实验的先后顺序,题目难度中等.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
下列离子方程式或化学反应方程式与所述事实相符且正确的是( )
| A、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO |
| B、将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol |
| C、向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1.下列说法正确的是( )
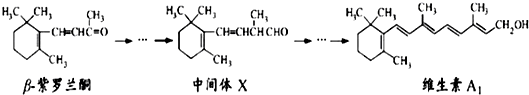

| A、β-紫罗兰酮可使酸性KMnO4溶液褪色 |
| B、1mol中间体X最多能与2molH2发生加成反应 |
| C、维生素A1不能氧化成醛 |
| D、维生素A1属于芳香族化合物 |
下列有关物质用途的说法正确的是( )
| A、单质硅常用做半导体材料和光导纤维,SiO2是人类将光能转化为电能的常用材料 |
| B、纯碱、烧碱、Al(OH)3等常用于治疗胃酸过多 |
| C、H2O2、Na2O2、氯水、漂白粉、84消毒液均可作漂白剂和消毒剂,且它们的漂白原理相同 |
| D、镁铝合金常用于制作窗框是因为它具有坚硬、密度小、溶点高、耐腐蚀等优良性能 |
下列溶液中,各组离子一定能大量共存的是( )
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
| D、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
 实验室里有一瓶试剂的标签部分被腐蚀,如图所示,仅知该试剂是只含短周期元素的纯净物.某同学设计实验探究该试剂成分,实验现象和结论都正确的是( )
实验室里有一瓶试剂的标签部分被腐蚀,如图所示,仅知该试剂是只含短周期元素的纯净物.某同学设计实验探究该试剂成分,实验现象和结论都正确的是( )| A、取该样品加入足量的硝酸钡溶液和稀盐酸,产生白色沉淀,则该样品的成分一定是硫酸钠 |
| B、取该样品溶于水,测得溶液pH=10,将溶液放置在空气中,一段时间后再测定溶液pH=7,该样品可能是亚硫酸钠 |
| C、取该样品溶于水,加入足量稀硫酸,将产生气体通入品红溶液,品红溶液褪色,加热溶液变红色,则样品成分是Na2S |
| D、若样品成分是硅酸钠(Na2SiO3),溶于水,滴加盐酸至过量,先生成白色沉淀,后沉淀溶解 |
 某同学设计了如下方案,来测定过氧化钠的样品的纯度(杂质不参加反应,条件为标准状况).
某同学设计了如下方案,来测定过氧化钠的样品的纯度(杂质不参加反应,条件为标准状况).
 )
)