题目内容
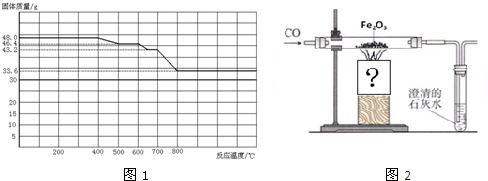
某研究小组模拟工业处理电镀含氰废水并测定处理的效率,利用如图所示装置进行实验.将CN-的浓度为0.2mol?L-1的含氰废水100mL与100mL NaClO溶液(过量)置于装置②三颈烧瓶中,充分反应.打开分液漏斗活塞,滴入100mL稀H2SO4,关闭活塞.

已知装置②中发生的主要反应依次为:
CN-+ClO-═CNO-+Cl-;2CNO-+2H++3C1O-═N2↑+2CO2↑+3C1-+H2O
(1)①和⑥的作用是 .
(2)装置②中,生成需由装置③除去的物质的离子方程式为 .
(3)反应结束后,缓缓通入空气的目的是 .
(4)为计算该实验中含氰废水被处理的百分率,需要测定 的质量.
(5)已知CN-的处理效率可高达90%,产生的CO2在标准状况下的体积为 .

已知装置②中发生的主要反应依次为:
CN-+ClO-═CNO-+Cl-;2CNO-+2H++3C1O-═N2↑+2CO2↑+3C1-+H2O
(1)①和⑥的作用是
(2)装置②中,生成需由装置③除去的物质的离子方程式为
(3)反应结束后,缓缓通入空气的目的是
(4)为计算该实验中含氰废水被处理的百分率,需要测定
(5)已知CN-的处理效率可高达90%,产生的CO2在标准状况下的体积为
考点:性质实验方案的设计
专题:实验题
分析:(1)实验的原理是利用CN-+ClO-═CNO+Cl-;2CNO-+2H++3ClO-═N2↑+2CO2↑+3Cl-+H2O,通过测定碱石灰的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率,实验中应排除空气中二氧化碳的干扰;
(2)酸性条件下,次氯酸根离子和氯离子反应生成氯气,氯气具有强氧化性,能氧化碘离子生成碘单质;
(3)反应结束后,缓缓通入空气,可将生成的二氧化碳全部被吸收;
(4)通过测定氢氧化钡溶液的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率;
(5)根据处理的CN-的物质的量,结合碳元素守恒可知被处理的CN-的物质的量为n(CN-)=n(CO2),原溶液中CN-的物质的量为0.1L×0.2mol/L=0.02mol,据此计算.
(2)酸性条件下,次氯酸根离子和氯离子反应生成氯气,氯气具有强氧化性,能氧化碘离子生成碘单质;
(3)反应结束后,缓缓通入空气,可将生成的二氧化碳全部被吸收;
(4)通过测定氢氧化钡溶液的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率;
(5)根据处理的CN-的物质的量,结合碳元素守恒可知被处理的CN-的物质的量为n(CN-)=n(CO2),原溶液中CN-的物质的量为0.1L×0.2mol/L=0.02mol,据此计算.
解答:
解:(1)实验的原理是利用CN-+ClO-═CNO+Cl-;2CNO-+2H++3ClO-═N2↑+2CO2↑+3Cl-+H2O,通过测定碱石灰的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率,实验中应排除空气中二氧化碳的干扰,防止对装置⑤实验数据的测定产生干扰,装置①和⑥的作用是排除空气中二氧化碳对实验的干扰,
故答案为:排除空气中二氧化碳对实验的干扰;
(2)根据已知装置②中发生的主要反应依次为CN-+ClO-═CNO-+Cl-、2CNO-+2H++3ClO-═N2↑+2CO2↑+3Cl-+H2O,可知溶液中有氯离子、氢离子和次氯酸根离子,酸性条件下,氯离子和次氯酸根离子反应生成氯气,产生的氯气用碘化钾吸收,所以发生的离子反应方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
(3)反应后装置中残留二氧化碳,应继续通过将净化的空气,将装置内的残留的二氧化碳全部进入装置⑤,以减少实验误差,
故答案为:使装置中残留的二氧化碳全部进入装置⑤;
(4)通过测定氢氧化钡溶液的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率,则需要测定装置⑤反应前后的质量,
故答案为:装置⑤反应前后质量;
(5)根据碳元素守恒可知被处理的CN-的物质的量为n(CN-)=n(CO2)=0.02mol×90%=0.018mol,所以标准状况下的体积为0.018mol×22.4L/mol=0.4L,
故答案为:0.4L.
故答案为:排除空气中二氧化碳对实验的干扰;
(2)根据已知装置②中发生的主要反应依次为CN-+ClO-═CNO-+Cl-、2CNO-+2H++3ClO-═N2↑+2CO2↑+3Cl-+H2O,可知溶液中有氯离子、氢离子和次氯酸根离子,酸性条件下,氯离子和次氯酸根离子反应生成氯气,产生的氯气用碘化钾吸收,所以发生的离子反应方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
(3)反应后装置中残留二氧化碳,应继续通过将净化的空气,将装置内的残留的二氧化碳全部进入装置⑤,以减少实验误差,
故答案为:使装置中残留的二氧化碳全部进入装置⑤;
(4)通过测定氢氧化钡溶液的质量的变化测得二氧化碳的质量,根据关系式计算含氰废水处理百分率,则需要测定装置⑤反应前后的质量,
故答案为:装置⑤反应前后质量;
(5)根据碳元素守恒可知被处理的CN-的物质的量为n(CN-)=n(CO2)=0.02mol×90%=0.018mol,所以标准状况下的体积为0.018mol×22.4L/mol=0.4L,
故答案为:0.4L.
点评:本题综合考查物质含量的测定的实验设计,以氯气的性质为载体考查化学实验设计和评价问题,题目难度中等,注意把握实验原理和实验方法.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
下列叙述正确的是( )
| A、NaCl溶液在电流的作用下电离出Na+ |
| B、离子化合物一定是电解质 |
| C、氨水呈弱碱性,故NH3是弱电解质 |
| D、溶于水电离出氢离子的化合物都是酸 |
将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为:CO2+2Mg=C+2MgO,该反应属于:①化合反应②分解反应③置换反应④复分解反应⑤氧化还原反应⑥离子反应⑦非氧化还原反应( )
| A、①③⑦ | B、③⑤ |
| C、②③⑥ | D、④⑥ |
下列说法正确的是( )
| A、电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 |
| B、能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动 |
| C、能层序数越大,s原子轨道的半径越大 |
| D、某微粒的最外层电子排布为2s22p6,则该微粒为Ne |
下列离子方程式书写正确的是( )
| A、铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag |
| B、铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| D、澄清石灰水与盐酸混合:Ca(OH)2+2H+=Ca2++2H2O |