题目内容
7.68g铜和一定量的浓硝酸反应,铜全部反应后,共收集到气体4.48L(标准状况下);
(1)该过程中发生了什么化学反应?写出发生反应的化学方程式,并计算说明.
(2)反应中共消耗硝酸多少摩尔.
(1)该过程中发生了什么化学反应?写出发生反应的化学方程式,并计算说明.
(2)反应中共消耗硝酸多少摩尔.
考点:化学方程式的有关计算
专题:计算题
分析:(1)根据n=
计算气体的物质的量,根据n=
计算Cu的物质的量,假设只生成NO或只生成NO2,根据电子转移守恒计算NO、NO2的物质的量,据此判断气体成分,确定发生的反应;
(2)根据N元素守恒,可知n(HNO3)=2n[Cu(NO3)2]+n(气体).
| V |
| Vm |
| m |
| M |
(2)根据N元素守恒,可知n(HNO3)=2n[Cu(NO3)2]+n(气体).
解答:
解:(1)气体物质的量=
=0.2mol,Cu的物质的量=
=0.12mol,
假设只生成NO,由电子转移守恒,则NO的物质的量为
=0.08mol,
若只生成NO2,由电子转移守恒,则NO2的物质的量为
=0.24mol,
由于0.08mol<0.2mol<0.24mol,故生成气体为NO、NO2的混合物,故发生反应:
Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,
故答案为:Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(2)根据N元素守恒,可知n(HNO3)=2n[Cu(NO3)2]+n(NO、NO2)=2×0.12mol+0.2mol=0.44mol,
答:反应中共消耗硝酸为0.44mol.
| 4.48L |
| 22.4L/mol |
| 7.68g |
| 64g/mol |
假设只生成NO,由电子转移守恒,则NO的物质的量为
| 0.12mol×2 |
| 5-2 |
若只生成NO2,由电子转移守恒,则NO2的物质的量为
| 0.12mol×2 |
| 5-4 |
由于0.08mol<0.2mol<0.24mol,故生成气体为NO、NO2的混合物,故发生反应:
Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,
故答案为:Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(2)根据N元素守恒,可知n(HNO3)=2n[Cu(NO3)2]+n(NO、NO2)=2×0.12mol+0.2mol=0.44mol,
答:反应中共消耗硝酸为0.44mol.
点评:本题考查化学方程式的有关计算,(1)中注意根据假设法判断气体成分,(2)中注意根据守恒思想进行解答,难度中等.

练习册系列答案
相关题目
下列反应属于氧化还原反应且焓变△H小于0的是( )
| A、Ba(OH)2?8H2O和NH4Cl反应 |
| B、Zn和稀H2SO4反应制氢气 |
| C、灼热的炭与水蒸气反应 |
| D、酸碱中和反应 |
一种常用融雪剂的主要成分的化学式为XY2,X原子的结构示意图为 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.下列说法正确的是( )
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.下列说法正确的是( )
 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.下列说法正确的是( )
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.下列说法正确的是( )| A、原子半径:X>Y>Z>W |
| B、气态氢化物的稳定性:Y>Z |
| C、最高价氧化物对应水化物的酸性:Y>W>Z |
| D、XY2和XW2都属于离子晶体,且所含的化学键类型均相同 |
A、B属于短周期元素,能以化学键结合成为AB2型的化合物,则B、A元素不可能分别属于周期表中的族数是( )
| A、ⅤA和ⅠA族 |
| B、ⅥA和ⅤA族 |
| C、ⅥA和ⅣA族 |
| D、ⅦA和ⅡA族 |
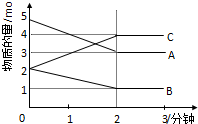 某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A、B、C均为气体).
某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A、B、C均为气体).
 如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.试回答下列问题:
如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.试回答下列问题: