题目内容
按要求作答:
(1)把FeCl3溶液加热蒸干,灼烧,最后得到的主要固体产物是 .原因是(用简要的文字和化学方程式来说明):
(2)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气.已知:N2(g)+2O2(g)═2NO2(g),△H=+67.7KJ?mol-1;N2H4(g)+O2(g)═N2(g)+2H2O (g),△H=-534KJ?mol-1则N2H4和NO2反应的热化学方程式为 .
(3)常温下,pH=13的Ba(OH)2溶液aL与PH=1的H2SO4溶液bL混合(混合后溶液体积变化忽略不计).若所得混合溶液PH=12,则a:b= .
(1)把FeCl3溶液加热蒸干,灼烧,最后得到的主要固体产物是
(2)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气.已知:N2(g)+2O2(g)═2NO2(g),△H=+67.7KJ?mol-1;N2H4(g)+O2(g)═N2(g)+2H2O (g),△H=-534KJ?mol-1则N2H4和NO2反应的热化学方程式为
(3)常温下,pH=13的Ba(OH)2溶液aL与PH=1的H2SO4溶液bL混合(混合后溶液体积变化忽略不计).若所得混合溶液PH=12,则a:b=
考点:盐类水解的应用,用盖斯定律进行有关反应热的计算,pH的简单计算
专题:化学反应中的能量变化,盐类的水解专题
分析:(1)根据三氯化铁在溶液中存在水解平衡,从平衡移动的角度分析并解答该题;
(2)根据盖斯定律,由已知热化学反应方程式乘以适当的系数进行加减构造目标热化学方程式,反应热也乘以相应的系数进行相应的加减,据此书写;
(3)若所得混合溶液pH=12,则碱过量,所以
=0.01mol/L,据此求出ab的比值.
(2)根据盖斯定律,由已知热化学反应方程式乘以适当的系数进行加减构造目标热化学方程式,反应热也乘以相应的系数进行相应的加减,据此书写;
(3)若所得混合溶液pH=12,则碱过量,所以
| a×0.1-b×0.1 |
| a+b |
解答:
解:(1)在FeCl3溶液中,Fe3+发生水解生成Fe(OH)3:溶液中存在水解平衡FeCl3+3H2O?Fe(OH)3+3HCl,由于加热蒸发,使HCl挥发,破坏平衡,使平衡不断向右移动,结果生成Fe(OH)3,又由于灼热发生2Fe(OH)3
Fe2O3+3H2O,使Fe(OH)3分解生成Fe2O3;
故答案为:Fe2O3;溶液中存在水解平衡FeCl3+3H2O?Fe(OH)3+3HCl,加热促进平衡正向移动,生成的氢氧化铁受热分解生成Fe2O3,2Fe(OH)3
Fe2O3+3H2O;
(2)已知:①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ?mol-l;
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ?mol-l;
由盖斯定律,②×2-①得2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g),故该反应的△H=2×(-534kJ?mol-1)-67.7kJ?mol-1)=-1135.7 kJ?mol-1,
即2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1,
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1;
(4)常温下,pH=13的Ba(OH)2溶液aL与PH=1的H2SO4溶液bL混合(混合后溶液体积变化忽略不计)若所得混合溶液pH=12,则碱过量,所以
=0.01mol/L,解得a:b=11:9,
故答案为:11:9.
| ||
故答案为:Fe2O3;溶液中存在水解平衡FeCl3+3H2O?Fe(OH)3+3HCl,加热促进平衡正向移动,生成的氢氧化铁受热分解生成Fe2O3,2Fe(OH)3
| ||
(2)已知:①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ?mol-l;
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ?mol-l;
由盖斯定律,②×2-①得2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g),故该反应的△H=2×(-534kJ?mol-1)-67.7kJ?mol-1)=-1135.7 kJ?mol-1,
即2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1,
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1;
(4)常温下,pH=13的Ba(OH)2溶液aL与PH=1的H2SO4溶液bL混合(混合后溶液体积变化忽略不计)若所得混合溶液pH=12,则碱过量,所以
| a×0.1-b×0.1 |
| a+b |
故答案为:11:9.
点评:本题考查了盐的水解原理的应用、盖斯定律的应用、酸碱混合pH的计算,题目难度中等,侧重于基础知识的应用的考查,注意对有关知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
| A、将混合气体通过盛有硫酸的洗气瓶 |
| B、将混合气体通过盛有足量溴水的洗气瓶 |
| C、将混合气体通过盛有酸性KMnO4溶液的洗气瓶 |
| D、将混合气体通过盛有澄清石灰水的洗气瓶 |
下列有关分类的说法正确的是( )
| A、CH3CH(CH3)2属于链状化合物 |
B、 属于芳香族化合物 属于芳香族化合物 |
C、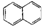 属于脂环化合物 属于脂环化合物 |
D、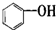 属于醇类化合物. 属于醇类化合物. |
在一定条件下发生下列反应,其中属于盐类水解反应的是( )
| A、NH4++2H2O?NH3?H2O+H3O+ |
| B、HCO3-+H2O?H3O++CO32- |
| C、Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ |
| D、CH3COOCH2CH3+H2O?CH3COOH+CH3CH2OH |
下列物质加入水中显著放热的是( )
| A、浓硫酸 |
| B、固体NaCl |
| C、无水乙醇 |
| D、固体NH4NO3 |
 如图是常见仪器的部分结构.
如图是常见仪器的部分结构.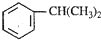 是一种重要的有机化工原料.根据题意完成下列
是一种重要的有机化工原料.根据题意完成下列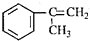 是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法
是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法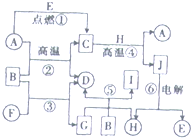 物质A~J之间的转化关系如图所示,其中A、F、H为常见的金属单质,D、E为常见的非金属气态单质,其余的为化合物,且单质E和单质F在点燃条件下可生成淡黄色固体,B在常温常压下为液态化合物.试回答下列问题:
物质A~J之间的转化关系如图所示,其中A、F、H为常见的金属单质,D、E为常见的非金属气态单质,其余的为化合物,且单质E和单质F在点燃条件下可生成淡黄色固体,B在常温常压下为液态化合物.试回答下列问题: