题目内容
下列各组离子在指定环境中一定能大量共存的是( )
| A、在含有大量I-离子的溶液中:Cl-、Fe3+、Na+、Mg2+ |
| B、在由水电离出的c(H+)=10-12mol?L-1 的溶液中:Na+、Ba2+、Cl-、Br- |
| C、使甲基橙呈红色的溶液中:Fe2+、Na+、SO42-、ClO- |
| D、在加入Al能放出大量H2的溶液中:NH4+、SO42-、Cl-、NO3- |
考点:离子共存问题
专题:
分析:A.I-具有还原性,I-和Fe3+发生氧化还原反应;
B.该溶液为酸性或碱性,和H+或OH-反应的离子不能存在;
C.使甲基橙呈红色的溶液呈酸性,HClO具有强氧化性,和Fe2+发生氧化还原反应;
D.在加入Al能放出大量H2的溶液为强酸性或强碱性,但不能含有NO3-.
B.该溶液为酸性或碱性,和H+或OH-反应的离子不能存在;
C.使甲基橙呈红色的溶液呈酸性,HClO具有强氧化性,和Fe2+发生氧化还原反应;
D.在加入Al能放出大量H2的溶液为强酸性或强碱性,但不能含有NO3-.
解答:
解:A.I-具有还原性,I-和Fe3+发生氧化还原反应,2I-+2Fe3+=2Fe2++I2,所以不能共存,故A错误;
B.该溶液为酸性或碱性,和H+或OH-反应的离子不能存在,这几种离子之间不反应且和和H+或OH-也不反应,所以能共存,故B正确;
C.使甲基橙呈红色的溶液呈酸性,HClO具有强氧化性,和Fe2+发生氧化还原反应而不能共存,2H++ClO-+2Fe2+=2Fe3++Cl-+H2O,故C错误;
D.在在加入Al能放出大量H2的溶液为强酸性或强碱性,但不能含有NO3-,HNO3和Al反应生成氮氧化物而不是H2,故D错误;
故选B.
B.该溶液为酸性或碱性,和H+或OH-反应的离子不能存在,这几种离子之间不反应且和和H+或OH-也不反应,所以能共存,故B正确;
C.使甲基橙呈红色的溶液呈酸性,HClO具有强氧化性,和Fe2+发生氧化还原反应而不能共存,2H++ClO-+2Fe2+=2Fe3++Cl-+H2O,故C错误;
D.在在加入Al能放出大量H2的溶液为强酸性或强碱性,但不能含有NO3-,HNO3和Al反应生成氮氧化物而不是H2,故D错误;
故选B.
点评:本题考查离子共存,离子之间不能发生氧化还原反应、不能发生双水解、不能生成气体、沉淀或弱电解质,还要结合题目限制条件分析解答,易错选项是D,注意酸性条件下,硝酸根离子和金属反应不生成氢气,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知CO(g)、H2(g)和CH3OH(l)的燃烧热(△H)分别为-283.0kJ?mol-1、-285.8kJ?mol-1和-726.5kJ?mol-1,则由CO(g)和H2(g)反应生成1molCH3OH(l)的△H 为( )
| A、-128.1 kJ?mol-1 |
| B、-411.1 kJ?mol-1 |
| C、-157.7 kJ?mol-1 |
| D、+157.7 kJ?mol-1 |
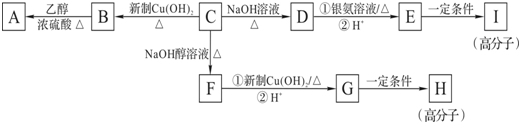
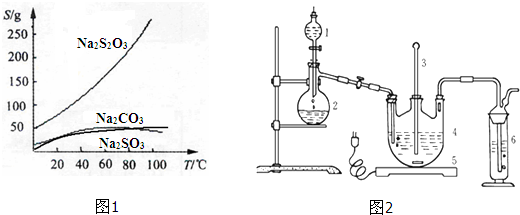


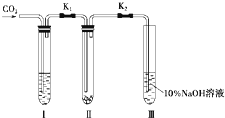 为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课题研究小组的同学们设计了如图的实验装置,分别进行了甲、乙两次实验:
为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课题研究小组的同学们设计了如图的实验装置,分别进行了甲、乙两次实验: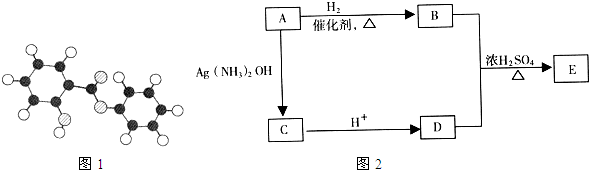
 A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验: