题目内容
对乙酰氨基苯酚(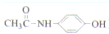 )(以下简称X)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧和关节痛、神经痛、偏头痛等病症,它可用如下方法来合成
)(以下简称X)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧和关节痛、神经痛、偏头痛等病症,它可用如下方法来合成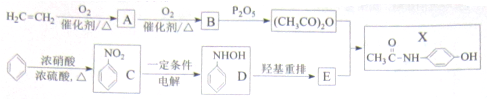
已知: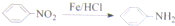 .请回答下列问题:
.请回答下列问题:
(1)下列有关E的说法正确的是
A.分子式为C6H6NO
B.能与溴水发生加成反应使其褪色
C.遇FeCl2溶液能发生显色反应
D.既能与NaOH溶液反应,又能与盐酸反应
(2)C→D的反应类型是 .
(3)一定条件下X与足量NaOH溶液反应的化学方程式 .
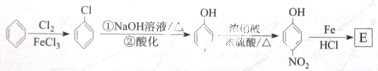
(4)某同学设计科以下途径合成E,试分析其合理性 (填“合理”或“不合理”).并说明理由 .
(5)写出满足下列条件的X的所有同分异构体的结构简式: .
①苯环上只有2种不同化学环境的氢原子;②苯环上连有-NH2;③属于酚类物质.
(6)以对二甲苯和乙烯为主要原料可合成涤纶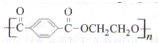 .请设计合成路线(无机试剂及溶剂任选) .
.请设计合成路线(无机试剂及溶剂任选) .
 )(以下简称X)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧和关节痛、神经痛、偏头痛等病症,它可用如下方法来合成
)(以下简称X)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧和关节痛、神经痛、偏头痛等病症,它可用如下方法来合成
已知:
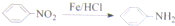 .请回答下列问题:
.请回答下列问题:(1)下列有关E的说法正确的是
A.分子式为C6H6NO
B.能与溴水发生加成反应使其褪色
C.遇FeCl2溶液能发生显色反应
D.既能与NaOH溶液反应,又能与盐酸反应
(2)C→D的反应类型是
(3)一定条件下X与足量NaOH溶液反应的化学方程式
(4)某同学设计科以下途径合成E,试分析其合理性

(5)写出满足下列条件的X的所有同分异构体的结构简式:
①苯环上只有2种不同化学环境的氢原子;②苯环上连有-NH2;③属于酚类物质.
(6)以对二甲苯和乙烯为主要原料可合成涤纶
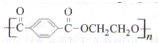 .请设计合成路线(无机试剂及溶剂任选)
.请设计合成路线(无机试剂及溶剂任选)考点:有机物的推断,有机物的合成,有机物的结构和性质
专题:有机物的化学性质及推断
分析:由转化关系可知,乙烯发生氧化反应生成A为CH3CHO,B为CH3COOH,苯发生硝化反应生成硝基苯,C→D加H去O,为还原反应,羟基重排生成E为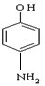 ,以此分析(1)-(3);
,以此分析(1)-(3);
(4)在催化剂条件下,苯和氯气发生取代反应生成氯苯,在催化剂条件下,氯苯水解生成B(苯酚),苯酚发生对位取代反应生成对硝基苯酚,发生还原反应生成 ;
;
(5)X的所有同分异构体满足①苯环上只有2种不同化学环境的氢原子;②苯环上连有-NH2;③属于酚类物质,则含2个对位取代基,苯环上只有2种H;
(6)对二甲苯和乙烯为主要原料可合成涤纶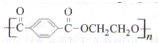 ,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,以此来解答.
,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,以此来解答.
 ,以此分析(1)-(3);
,以此分析(1)-(3);(4)在催化剂条件下,苯和氯气发生取代反应生成氯苯,在催化剂条件下,氯苯水解生成B(苯酚),苯酚发生对位取代反应生成对硝基苯酚,发生还原反应生成
 ;
;(5)X的所有同分异构体满足①苯环上只有2种不同化学环境的氢原子;②苯环上连有-NH2;③属于酚类物质,则含2个对位取代基,苯环上只有2种H;
(6)对二甲苯和乙烯为主要原料可合成涤纶
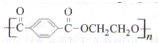 ,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,以此来解答.
,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,以此来解答.解答:
解:由转化关系可知,乙烯发生氧化反应生成A为CH3CHO,B为CH3COOH,苯发生硝化反应生成硝基苯,C→D加H去O,为还原反应,羟基重排生成E为 ,
,
(1)A.E为 ,分子式为C6H7NO,故A错误;
,分子式为C6H7NO,故A错误;
B.含酚-OH,能与溴水发生取代反应生成白色沉淀,故B错误;
C.含酚-OH,遇FeCl3溶液能发生显色反应,故C正确;
D.含酚-OH具有酸性,含氨基具有碱性,则既能与NaOH溶液反应,又能与盐酸反应,故D正确;
故答案为:CD;
(2)由上述分析可知,C→D的反应类型是还原反应,故答案为:还原反应;
(3)X与足量NaOH溶液反应的化学方程式为 ,
,
故答案为: ;
;
(4)给出的流程为在催化剂条件下,苯和氯气发生取代反应生成氯苯,在催化剂条件下,氯苯水解生成B(苯酚),苯酚发生对位取代反应生成对硝基苯酚,发生还原反应生成 ,但氯苯水解后再硝化,苯酚易被氧化,则不合理,
,但氯苯水解后再硝化,苯酚易被氧化,则不合理,
故答案为:不合理;氯苯水解后再硝化,苯酚易被氧化;
(5)X的所有同分异构体满足①苯环上只有2种不同化学环境的氢原子;②苯环上连有-NH2;③属于酚类物质,则含2个对位取代基,苯环上只有2种H,符合条件的结构简式为 ,
,
故答案为: ;
;
(6)对二甲苯和乙烯为主要原料可合成涤纶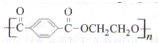 ,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,则合成流程为
,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,则合成流程为 ,
,
故答案为: .
.
 ,
,(1)A.E为
 ,分子式为C6H7NO,故A错误;
,分子式为C6H7NO,故A错误; B.含酚-OH,能与溴水发生取代反应生成白色沉淀,故B错误;
C.含酚-OH,遇FeCl3溶液能发生显色反应,故C正确;
D.含酚-OH具有酸性,含氨基具有碱性,则既能与NaOH溶液反应,又能与盐酸反应,故D正确;
故答案为:CD;
(2)由上述分析可知,C→D的反应类型是还原反应,故答案为:还原反应;
(3)X与足量NaOH溶液反应的化学方程式为
 ,
,故答案为:
 ;
;(4)给出的流程为在催化剂条件下,苯和氯气发生取代反应生成氯苯,在催化剂条件下,氯苯水解生成B(苯酚),苯酚发生对位取代反应生成对硝基苯酚,发生还原反应生成
 ,但氯苯水解后再硝化,苯酚易被氧化,则不合理,
,但氯苯水解后再硝化,苯酚易被氧化,则不合理,故答案为:不合理;氯苯水解后再硝化,苯酚易被氧化;
(5)X的所有同分异构体满足①苯环上只有2种不同化学环境的氢原子;②苯环上连有-NH2;③属于酚类物质,则含2个对位取代基,苯环上只有2种H,符合条件的结构简式为
 ,
,故答案为:
 ;
;(6)对二甲苯和乙烯为主要原料可合成涤纶
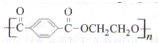 ,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,则合成流程为
,由逆合成法可知,对苯二甲酸与乙二醇发生缩聚反应合成,由对而甲苯发生氧化反应生成对苯二甲酸,由乙烯发生加成、水解反应制备乙二醇,则合成流程为 ,
,故答案为:
 .
.
点评:本题考查有机物的推断和合成,为高频考点,把握合成流程这发生的反应、官能团的变化、有机物结构与性质为解答的关键,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、只有一种元素组成的物质,一定是纯净物 |
| B、酸性氧化物一定都是非金属氧化物 |
| C、非金属元素组成的化合物一定含有共价键 |
| D、阴阳离子中均分别只含有一种元素,则由这样的阴阳离子组成的物质一定是纯净物 |
下列叙述正确的是( )
| A、Fe在氯气中燃烧生成FeCl2 |
| B、SiO2的化学性质不活泼,不与任何酸发生反应 |
| C、常温下,铝制品用浓硫酸或浓硝酸处理过,可耐腐蚀 |
| D、铁粉中混有铝粉既可用过量的NaOH溶液,也可以用过量FeCl3溶液充分反应过滤除去 |
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示)下列有关说法正确的是(  )
)
 )
)| A、氯碱工业是指以电解烙融NaCl为基础取Cl2等产品的工业 |
| B、流程②中结晶出的MgCl2?6H2O可在空气中受热分解制无水MgCl2 |
| C、在流程③④⑤中溴元素均被氧化 |
| D、流程①中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸 |
下列关系式错误的是( )
| A、等浓度的HCN溶液NaCN溶液等体积混合,所得溶液pH>7,则溶液中离子浓度:c(Na+ )>c(CN-)>c(OH- )>c(H+ ) | ||||
| B、0.4mol?L-1某一元酸HA溶液和0.2 mol?L-1NaOH溶液等体积混合的溶液中:2c(OH- )+c(A- )=2c(H+ )+c(HA) | ||||
| C、常温下等浓度的Na2SO3与NaHSO3溶液等体积混合后溶液的pH=7.2,调整比例当溶液呈中性时:c(Na+ )>c(HSO3-)>c(SO32-)>c(H+ )═c(OH- ) | ||||
D、两种弱酸HX和HY混合后,溶液中的c(H+ )为(Ka为电离平衡常数):c(H+ )=
|
下列有关溶液的说法正确的是( )
| A、物质的量浓度相等的NH4Al(SO4)2、NH4HCO3、NH4Cl溶液中c(NH4+):NH4HCO3>NH4Cl>NH4Al(SO4)2 |
| B、1.0mol?L-1Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C、测得酸式盐NaHA溶液的PH=3,则NaHA在溶液中一定是电离大于水解 |
| D、某二元弱酸的酸式盐NaHA溶液中:c(Na+)=c(HA-)+c(H2A)+c(A2-)+c(OH-) |
实验室保存下列药品的方法不正确的是( )
| A、氢氟酸保存在密封的玻璃瓶中 |
| B、少量金属钠保存在煤油中 |
| C、硅酸钠保存在带橡皮塞的试剂瓶中 |
| D、氢氧化钠溶液保存在带橡皮塞的试剂瓶中 |
已知:C(s)+CO2(g)═2CO(g)△H>0,该反应达到平衡后,改变下列条件都有利于反应向正方向进行的是( )
| A、升高温度和减小压强 |
| B、降低温度和减小压强 |
| C、降低温度和增大压强 |
| D、升高温度和增大压强 |
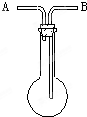 洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体:
洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体: